题目内容
下列各组离子能大量共存于同一溶液中,且加入过量NaOH溶液或少量稀H2SO4时,都能产生白色沉淀的是
| A.Ba2+、Mg2+、NO3-、CO32- | B.Na+、Al3+、Cl-、AlO2- |
| C.Ba2+、K+、Cl-、HCO3- | D.NH4+、Fe3+、Ba2+、Cl- |
C
解析试题分析:A.因Ba2+、Mg2+分别与CO32-结合生成沉淀,则不能共存,故A错误;B.因Al3+、AlO2-相互促进水解而不能共存,故B错误;C.因该组离子之间不反应,能共存,加NaOH溶液与Ba2+、HCO3-反应生成碳酸钡白色沉淀,加硫酸生成硫酸钡白色沉淀,故C正确;D.该组离子之间不反应,能共存,但加入NaOH与Fe3+反应生成红褐色沉淀,加硫酸生成硫酸钡白色沉淀,故D错误;
考点:本题考查离子的共存,熟悉复分解反应发生的条件及常见离子之间的反应即可解答,选项C为解答的易错点,并注意沉淀的颜色来解答,题目难度不大.

练习册系列答案
相关题目
下列物质中,属于电解质的是( )
| A.碳酸钙 | B.石墨 | C.酒精 | D.氯化钠溶液 |
下列离子方程式正确的是( )。
A.三氯化铝溶液中加入过量氨水: |
B. 的NaAlO2溶液和 的NaAlO2溶液和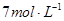 的HCI等体积互相均匀混合: 的HCI等体积互相均匀混合: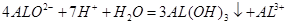 |
C.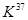 ClO3与浓盐酸(HCI)在加热时生成氯气: ClO3与浓盐酸(HCI)在加热时生成氯气: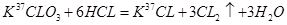 |
D.将25mL 0.l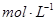 盐酸缓缓滴入25mL 0.1 盐酸缓缓滴入25mL 0.1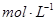 Na2CO3溶液中,并不断搅拌: Na2CO3溶液中,并不断搅拌: |
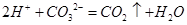
下列各组离子在溶液中能大量共存的是
| A.Cu2+、Mg2+、SO42-、Cl- | B.Na+、H+、Fe3+、NO3- |
| C.Ba2+、K+、SO42-、Cl- | D.Na+、Ca2+、HCO3-、OH- |
下列离子方程式书写正确的是
| A.NaHCO3溶液中加入NaOH 溶液:HCO3—+OH—=CO2↑+H2O |
| B.在NaOH溶液中滴入少量AlC13溶液:Al3++3OH—=Al(OH)3↓ |
| C.甲酸溶液中滴入NaOH溶液:HCOOH+OH—=HCOO—+H2O |
| D.CO2通入CaCl2溶液:CO2+H2O+Ca2+=CaCO3↓+2H+ |
下列离子方程式表示正确的是( )
| A.AgNO3溶液中加入Cu:Cu + Ag+ = Cu2+ + Ag |
| B.NaHSO4溶液与Ba(OH)2溶液反应至中性:H++SO42—+Ba2++OH—=BaSO4↓+H2O |
| C.甲酸溶液滴到大理石台板上有气泡产生:2H+ + CaCO3 = CO2↑+ Ca2+ + H2O |
| D.等体积等物质的量浓度的NaHCO3和Ba(OH)2溶液混合: |
某硝石(主要成分是NaNO3)除去不溶性杂质后,其溶液中还含有NaCl、Ca(HCO3)2,实验室提纯NaNO3溶液时,往溶液中依次加入过量的NaOH、AgNO3、Na2CO3,过滤后再加入适量硝酸。以上过程发生5个离子反应,以下4个离子方程式中不符合反应事实的是
| A.Ca2++HCO3-+OH-→ CaCO3↓+H2O | B.Ag++OH-→AgOH↓ |
| C.2Ag++CO32-→Ag2CO3↓ | D.CO32-+2H+→ CO2↑+H2O |
下列说法正确的是
| A.浓盐酸在化学反应中既可以做氧化剂,又可以作还原剂 |
B.在任何条件下都不能发生Cu+H2SO4=CuSO4+H2 反应 反应 |
| C.浓度和体积相同的FeBr2、FeI2溶液中,分别通入少量氯气都首先发生置换反应 |
| D.二氧化氮与水反应的离子方程式是3NO2+H2O=2HNO3+NO |
