题目内容
【题目】下列物质中,不属于合金的是
A. 水银B. 硬铝C. 青铜D. 碳素钢
【答案】A
【解析】
由两种或两种以上的金属或金属与非金属熔合而成的具有金属特性的物质是合金,硬铝是一种铝合金、青铜是Cu—Sn合金、碳素钢是含碳量为0.03%~2%的铁碳合金,水银是金属单质,不是合金,答案选A。

 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案 启东小题作业本系列答案
启东小题作业本系列答案【题目】下列实验操作规范且能达到实验目的的是
实验目的 | 实验操作 | |
A | 称取2.0gNaOH固体 | 先在两盘上各放一张滤纸,然后右盘添加2g砝码,左盘加入NaOH至两盘平衡 |
B | 除去CO2中的SO2 | 将混合气体通入饱和Na2CO3溶液中 |
C | 证明Na2CO3溶液中存在水解平衡 | 向含有酚酞的Na2CO3溶液中滴加CaCl2溶液,观察颜色变化 |
D | 测定硫酸浓度 | 向洁净的锥形瓶中加入20.00mL待测硫酸,用0.1000mol/L的NaOH标准液滴定 |
A. A B. B C. C D. D
【题目】用NH3催化还原NxOy可以消除氮氧化物的污染.
已知:反应Ⅰ:4NH3(g)+6NO(g)5N2(g)+6H2O(l)△H1
反应Ⅱ:2NO(g)+O2(g)2NO2(g)△H2 (且|△H1|=2|△H2|)
反应Ⅲ:4NH3(g)+6NO2(g)5N2(g)+3O2(g)+6H2O(l)△H3
反应I和反应II在不同温度时的平衡常数及其大小关系如表
温度/K | 反应I | 反应II | 已知: |
298 | K1 | K2 | |
398 | K1′ | K2′ |
(1)推测反应Ⅲ是反应(填“吸热”或“放热”)
(2)相同条件下,反应I在2L密闭容器内,选用不同的催化剂,反应产生N2的量随时间变化如图所示.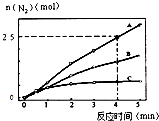
①计算0~4分钟在A催化剂作用下,反应速率v(NO)=
②下列说法正确的是 .
A.该反应的活化能大小顺序是:Ea(A)>Ea(B)>Ea(C)
B.增大压强能使反应速率加快,是因为增加了活化分子百分数
C.单位时间内H﹣O键与N﹣H键断裂的数目相等时,说明反应已经达到平衡
D.若在恒容绝热的密闭容器中发生反应,当K值不变时,说明反应已经达到平衡
(3)一定条件下,反应II达到平衡时体系中n(NO):n(O2):n(NO2)=2:1:2.在其它条件不变时,再充入NO2气体,分析NO2体积分数﹣﹣φ(NO2)的变化情况:(填“变大”、“变小”或“不变”)恒温恒压容器,φ(NO2);恒温恒容容器,φ(NO2) .
(4)一定温度下,反应III在容积可变的密闭容器中达到平衡,此时容积为3L,c(N2)与反应时间t变化曲线X如图所示,若在t1时刻改变一个条件,曲线X变为曲线Y或曲线Z.则: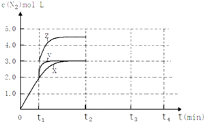
①变为曲线Y改变的条件是 . 变为曲线Z改变的条件是
②若t2降低温度,t3达到平衡,请在图中画出曲线X在t2﹣t4内 c(N2)的变化曲线.