题目内容
【题目】煤的液化可以合成甲醇。下列有关说法正确的是
①“气化”:C(s)+2H2O(g)![]() CO2(g)+2H2(g) ΔH1=+90.1 kJ·mol-1
CO2(g)+2H2(g) ΔH1=+90.1 kJ·mol-1
②催化液化Ⅰ:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ΔH2=-49.0 kJ·mol-1
CH3OH(g)+H2O(g) ΔH2=-49.0 kJ·mol-1
③催化液化Ⅱ:CO2(g)+2H2(g)![]() CH3OH(g)+1/2O2(g) ΔH3=a kJ·mol-1
CH3OH(g)+1/2O2(g) ΔH3=a kJ·mol-1

A. 催化液化Ⅰ中使用催化剂,反应的活化能Ea、ΔH2都减小
B. 反应C(s)+H2O(g)+H2(g)![]() CH3OH(g) ΔH=+41.1 kJ·mol-1
CH3OH(g) ΔH=+41.1 kJ·mol-1
C. ΔH2>ΔH3
D. 如图为甲醇燃料电池的工作原理示意图,负极的电极反应为CH3OH-6e-+6OH-![]() CO2↑+5H2O
CO2↑+5H2O
【答案】B
【解析】
A. 催化液化Ⅰ中使用催化剂,反应的活化能Ea减小但ΔH2不变,故错误;B. ①“气化”:C(s)+2H2O(g)![]() CO2(g)+2H2(g) ΔH1=+90.1 kJ·mol-1,②催化液化Ⅰ:CO2(g)+3H2(g)
CO2(g)+2H2(g) ΔH1=+90.1 kJ·mol-1,②催化液化Ⅰ:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ΔH2=-49.0 kJ·mol-1,根据盖斯定律分析,①+②可得热化学方程式为:反应C(s)+H2O(g)+H2(g)
CH3OH(g)+H2O(g) ΔH2=-49.0 kJ·mol-1,根据盖斯定律分析,①+②可得热化学方程式为:反应C(s)+H2O(g)+H2(g)![]() CH3OH(g) ΔH=+90.1kJ/mol-49.0kJ/mol=+41.1 kJ·mol-1,故正确;C. ②催化液化Ⅰ:CO2(g)+3H2(g)
CH3OH(g) ΔH=+90.1kJ/mol-49.0kJ/mol=+41.1 kJ·mol-1,故正确;C. ②催化液化Ⅰ:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ΔH2=-49.0 kJ·mol-1,③催化液化Ⅱ:CO2(g)+2H2(g)
CH3OH(g)+H2O(g) ΔH2=-49.0 kJ·mol-1,③催化液化Ⅱ:CO2(g)+2H2(g)![]() CH3OH(g)+1/2O2(g) ΔH3=a kJ·mol-1,根据盖斯定律分析,②-③可得热化学方程式为:H2(g) +1/2O2(g)= H2O(g) ΔH=ΔH2-ΔH3=(-49.0-a) kJ·mol-1,该反应为放热反应,即ΔH <0,则有ΔH2-ΔH3<0,即ΔH2<ΔH3,故错误;D. 如图为甲醇燃料电池的工作原理示意图,负极的电极反应为CH3OH-6e-+8OH-
CH3OH(g)+1/2O2(g) ΔH3=a kJ·mol-1,根据盖斯定律分析,②-③可得热化学方程式为:H2(g) +1/2O2(g)= H2O(g) ΔH=ΔH2-ΔH3=(-49.0-a) kJ·mol-1,该反应为放热反应,即ΔH <0,则有ΔH2-ΔH3<0,即ΔH2<ΔH3,故错误;D. 如图为甲醇燃料电池的工作原理示意图,负极的电极反应为CH3OH-6e-+8OH-![]() CO32-+6H2O,故错误。故选B。
CO32-+6H2O,故错误。故选B。

 阅读快车系列答案
阅读快车系列答案【题目】某化学小组采用类似制乙酸乙酯的装置,用环己醇制备环己烯:
已知: 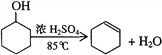
密度(g/cm3) | 熔点(℃) | 沸点(℃) | 溶解性 | |
环己醇 | 0.96 | 25 | 161 | 能溶于水 |
环己烯 | 0.81 | -103 | 83 | 难溶于水 |
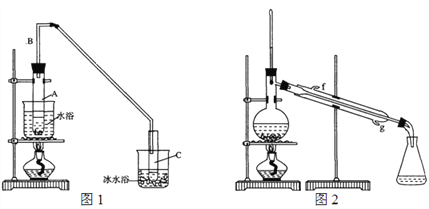
(1)制备粗品:采用如图1所示装置,用环己醇制备环己烯。
将12.5 mL环己醇加入试管A中,再加入1 mL浓硫酸,摇匀放入碎瓷片,缓慢加热至反应完全,在试管C内得到环己烯粗品。
①A中碎瓷片的作用是_____________,导管B的作用是_______________。
②试管C置于冰水浴中的目的是________________________。
(2)制备精品:
①环己烯粗品中含有环己醇和少量有机酸性杂质等。加入饱和食盐水,振荡、静置、分层,环己烯在______层(填“上”或“下”),分液后用________洗涤(填字母)。
A. KMnO4溶液 B. 稀H2SO4 C. Na2CO3溶液
②再将环己烯按图2装置蒸馏,冷却水从____口(填字母)进入。蒸馏时加入生石灰,目的是______________________________________。
③收集产品时,控制的温度应在______左右,实验制得的环己烯精品质量低于理论产量,可能的原因是______(填字母)。
a. 蒸馏时从70℃开始收集产品
b. 环己醇实际用量多了
c. 制备粗品时环己醇随产品一起蒸出
(3)以下区分环己烯精品和粗品的方法,合理的是________(填字母)。
a. 用酸性高锰酸钾溶液
b. 用金属钠
c. 测定沸点
【题目】I 有一种有机物X,其结构简式为:HO—CH2CH=CH—COOH,试回答下列问题:
(1)X中的含氧官能团名称是_______________、_______________。
(2)向X中加入金属钠,将发生反应的化学方程式是_______________。
(3)如果在X中加入NaOH溶液,将发生反应的化学方程式是___________。
(4)下列关于X的说法中正确的是________________。
①X既能与酸发生酯化反应,又能与醇发生酯化反应
②X能够使溴水褪色,但不能使KMnO4酸性溶液褪色
③X能够发生缩聚反应,但不能发生加聚反应
II.分子式为C3H6O2的有机物有多种同分异构体,现有其中的四种X、Y、Z、W,它们的分子中均含甲基,将它们分别进行下列实验以鉴别,其实验记录如下:
NaOH溶液 | 银氨溶液 | 新制Cu(OH)2 | 金属钠 | |
X | 中和反应 | 无现象 | 溶解 | 产生氢气 |
Y | 无现象 | 有银镜 | 加热后有砖红色沉淀 | 产生氢气 |
Z | 水解反应 | 有银镜 | 加热后有砖红色沉淀 | 无现象 |
W | 水解反应 | 无现象 | 无现象 | 无现象 |
回答下列问题:
(1)写出X的结构简式________, W的系统命名是________.
(2)①Y在一定条件下发生分子内的脱水反应的化学方程式________________
②Z与NaOH溶液反应的化学方程式_______________________________