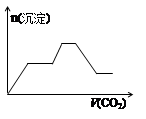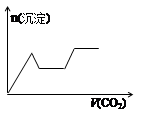题目内容
无机化合物可根据其组成和性质进行分类。
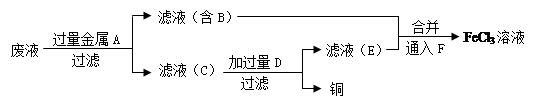
(1)如图所示的物质分类方法是 。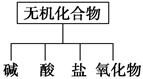
(2)以Na、K、H、O、C、S、N中任两种或三种元素组成合适的物质,分别填在下表②③⑥的后面。
| 物质类别 | 酸 | 碱 | 盐 | 氧化物 |
| 化学式 | ①HCl ② | ③ ④Ba(OH)2 | ⑤Na2CO3 ⑥ | ⑦CO2 ⑧Na2O2 |
(3)写出⑦转化为⑤的化学方程式: 。
(4)呼吸面具中用⑧作为O2来源的反应原理为: 。
(5)实验室制备⑦常用 和 反应,检验该气体的方法是 。
(1)树状分类法
(2)②H2SO4 ③NaOH ⑥K2CO3(合理即可)
(3)2NaOH+CO2=Na2CO3+H2O
(4)2Na2O2+2CO2=2Na2CO3+O2(或2Na2O2+2H2O=4NaOH+O2↑)
(5)CaCO3 稀盐酸 把生成的无色无味气体通入澄清石灰水,若变浑浊,则生成的气体为CO2
解析

练习册系列答案
 一课一练课时达标系列答案
一课一练课时达标系列答案
相关题目
下列物质分类正确的一组是
| | A | B | C | D |
| 电解质 | 浓硫酸 | 胆矾 | 硫酸钡 | 冰醋酸 |
| 混合物 | 漂白粉 | 淀粉 | 水玻璃 | 冰水混合物 |
| 酸性氧化物 | SO2 | Mn2O7 | SiO2 | NO2 |
| 酸 | HClO4 | H2SiO3 | NaHSO4 | CH3COOH |
下列说法不正确的是
| A.“光化学烟雾”“硝酸型酸雨”的形成都与氮氧化合物有关 |
| B.根据分散质微粒直径大小可以将分散系分为溶液、胶体和浊液 |
| C.SiO2可用于制造光导纤维,其性质稳定,不溶于强酸、强碱 |
| D.焰火的五彩缤纷是某些金属元素的性质的展现 |
硫酸亚铁是一种重要的化工原料,可以制备一系列物质。下列说法错误的是( )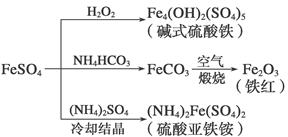
| A.碱式硫酸铁水解能产生Fe(OH)3胶体,可用作净水剂 |
| B.为防止NH4HCO3分解,生产FeCO3需在较低温度下进行 |
| C.可用KSCN溶液检验(NH4)2Fe(SO4)2是否被氧化 |
| D.常温下,(NH4)2Fe(SO4)2在水中的溶解度比FeSO4的大 |
I .用序号回答下列各题:
① 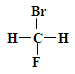 和
和 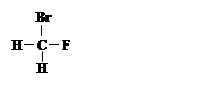
②1H—、2H、3H +、D2 ③淀粉和纤维素
④ 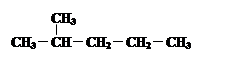 和
和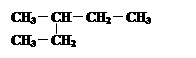
⑤16O2、18O3 ⑥235U、238U
其中互为同位素的是 。
互为同素异形体的是 。
互为同分异构体的是 。
是同一种化合物的是 。
II. 请选择合适的试剂检验某物质中是否含括号内物质:
| 序号 | 原物质(需检验物质) | 试剂 |
| ① | CO2(SO2) | |
| ② | 乙醇(水) | |
| ③ | 直馏汽油( 裂化汽油) | |
Ⅲ.某元素R气态氢化物化学式为HnR。若最高价氧化物对应水化物分子中有b个氧原子,则其最高价氧化物对应水化物化学式通常表达为 。(含n和b)