题目内容
8.对于任何一个平衡体系,采取下列措施一定会引起平衡移动的是( )| A. | 加入一种反应物 | B. | 增加体系的压强 | C. | 升高温度 | D. | 使用催化剂 |
分析 影响平衡移动的因素只有温度、浓度和压强三方面因素,当改变影响平衡的一个条件,平衡向减弱这种改变的方向移动,据此分析.
解答 解:A、在反应中,加入一种固体反应物,固体量的增减不会引起化学平衡的移动,故A错误;
B、对于没有气体参加的反应,或是前后气体体积不变的反应,压强不会引起平衡的移动,故B错误;
C、任何化学反应一定伴随能量的变化,升高温度,化学平衡一定是向着吸热方向进行,故C正确;
D、使用催化剂只能改变化学反应的速率,不会引起化学平衡的移动,故D错误.
故选C.
点评 本题考查学生影响化学平衡移动的因素,注意每个因素的使用情况是解答的关键.

练习册系列答案
相关题目
18.某有机物的结构简式如图所示,关于该物质的叙述错误的是( )
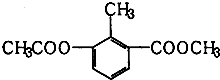

| A. | 一个分子中含有12个H原子 | B. | 该物质属于芳香族化合物 | ||
| C. | 能使酸性KMnO4溶液褪色 | D. | 苯环上的一氯代物有2种 |
19.${\;}_{6}^{13}$C-NMR(核磁共振)可以用于含碳化合物的结构分析,${\;}_{6}^{13}$C表示的碳原子( )
| A. | 核外有13个电子,其中6个能参与成键 | |
| B. | 核内有6个质子,核外有7个电子 | |
| C. | 质量数为13,原子序数为6,核内有7个质子 | |
| D. | 质量数为13,原子序数为6,核内有7个中子 |
16.铜~锌原电池如图所示,电解质溶液为稀硫酸,下列说法不正确的是( )
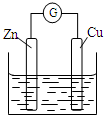

| A. | 铜电极上发生还原反应 | B. | 锌电极是原电池的负极 | ||
| C. | 电子从铜极经过外电路流向锌极 | D. | 锌电极上的反应为Zn-2e-═Zn2+ |
3.下列反应中,不属于加成反应的是( )
| A. | 乙炔与氯化氢反应制取氯乙烯 | B. | 乙烯使溴的四氯化碳溶液褪色 | ||
| C. | 乙醛与氢气反应生成乙醇 | D. | 苯与液溴在铁催化作用下反应 |
13.下列变化属于化学变化的是( )
| A. | 氨的液化 | B. | 氯化铵受热“升华” | ||
| C. | 碘的升华 | D. | 硝酸的挥发 |
20.根据有机化合物的命名原则,下列命名正确的是( )
| A. | 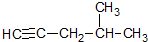 4-甲基-1,2-戊炔 4-甲基-1,2-戊炔 | |
| B. | CH3 CH (CH3)CH=CHCH32-甲基-3-戊烯 | |
| C. | 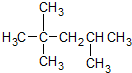 2,2,3-甲基戊烷 2,2,3-甲基戊烷 | |
| D. | 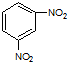 间二硝基苯 间二硝基苯 |
17.根据如图所示的N2(g)和O2(g)反应生成NO(g)过程中能量变化情况,判断下列说法正确的是( )

| A. | 该反应中反应物所具有的总能量高于生成物所具有的总能量 | |
| B. | 2 mol N原子结合生成N2(g)时需要放出946 kJ能量 | |
| C. | 1 mol NO(g)分子中的化学键断裂时需要放出632 kJ能量 | |
| D. | 该反应的热化学方程式为:N2+O2═2NO△H=+180 kJ/mol. |
18.已知有机物甲、乙、丙有如下信息:
据此推断:
(1)甲的分子式为C3H8,若甲分子中有2个氢原子被F原子取代,所得的有机产物可能有4种.
(2)乙是性能优良的环保产物,可代替某些破坏臭氧层的氟利昂产品用作制冷剂.其分子中C、H、F的原子个数之比为1:2:2,则乙的结构式为 .
.
(3)将甲、乙按物质的量之比1:1混合,所得混合物的平均摩尔质量等于丙的摩尔质量,且丙分子不存在同分异构体,则丙的分子式为C2H5F.
| 甲 | 乙 | 丙 | |
| 所含元素 | C、H | C、H、F | C、H、F |
| 所含电子数 | 26 | ||
| 结构特点 | 饱和有机物 | ||
(1)甲的分子式为C3H8,若甲分子中有2个氢原子被F原子取代,所得的有机产物可能有4种.
(2)乙是性能优良的环保产物,可代替某些破坏臭氧层的氟利昂产品用作制冷剂.其分子中C、H、F的原子个数之比为1:2:2,则乙的结构式为
 .
.(3)将甲、乙按物质的量之比1:1混合,所得混合物的平均摩尔质量等于丙的摩尔质量,且丙分子不存在同分异构体,则丙的分子式为C2H5F.