题目内容
【题目】一定条件下,在体积为10 L的固定容器中发生反应:N2(g)+3H2(g)![]() 2NH3(g) ΔH<0,反应过程如图,下列说法正确的是
2NH3(g) ΔH<0,反应过程如图,下列说法正确的是
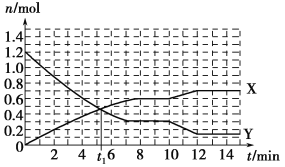
A.t1 min时正、逆反应速率相等
B.X曲线表示NH3的物质的量随时间变化的关系
C.0~8 min,H2的平均反应速率v(H2)=0.01 mol·L-1·min-1
D.10~12 min,升高温度使反应速率加快,平衡正向移动
【答案】B
【解析】
试题分析:A.t1 min时反应物、生成物的物质的量相等,但是不能表示正、逆反应速率相等,错误。B.X表示的是生成物,由于生成物只有NH3,因此X曲线表示NH3的物质的量随时间变化的关系,正确。C.0~8 min,NH3变化的物质的量是0.6mol,则H2变化的物质的量是0.9mol,所以H2的平均反应速率v(H2)=0.9mol ÷10L÷8min=0.01125 mol·L-1·min-1,错误。D.10~12 min,改变条件,是反应速率加快,产生更多的NH3,若是升高温度使反应速率加快,由于该反应的正反应是放热反应,升高温度,平衡逆向移动,错误。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
【题目】用下图装置进行下列实验:将①中溶液滴入②中,预测的现象与实际相符的是
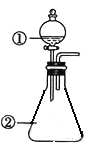
选项 | ①中物质 | ②中物质 | 预测②中的现象 |
A | 稀盐酸 | 碳酸钠与氢氧化钠的混合溶液 | 立即产生气泡 |
B | 浓硝酸 | 用砂纸打磨过的铝条 | 产生红棕色气体 |
C | 草酸溶液 | 高锰酸钾酸性溶液 | 溶液逐渐褪色 |
D | 液溴 | 苯 | 生成白雾 |
A. A B. B C. C D. D