题目内容
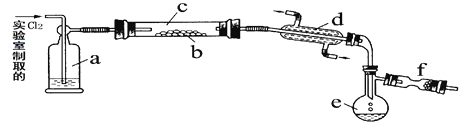
【题目】(14分)氯化硫(S2Cl2)是一种黄红色液体,有刺激性、窒息性恶臭,熔点为-80℃,沸点137.1℃。在空气中强烈发烟,易与水发生水解反应。人们使用它作橡胶硫化剂,使橡胶硫化,改变生橡胶热发粘冷变硬的不良性能。在熔融的硫中通入氯气即可生成S2Cl2。下图是实验室用S和Cl2制备S2Cl2的装置(夹持装置、加热装置均已略去)。
(1)已知S2Cl2分子结构与H2O2相似,请写出S2Cl2的电子式 。
(2)装置a中应放试剂为 ,其作用为 ;装置c为何水平放置 ;
(3)该实验的操作顺序应为 (用序号表示)。
①加热装置c ②通入Cl2③通冷凝水 ④停止通Cl2⑤停止加热装置c
(4)f装置中应放置的试剂为 ,其作用为 。
(5)已知S2Cl2水解时,只有一种元素的化合价发生了变化,且被氧化和被还原的该元素的物质的量之比为1:3,请写出该反应的化学方程式 。
【答案】(1)![]() (2分) (2) 浓H2SO4(1分)干燥Cl2(1分)
(2分) (2) 浓H2SO4(1分)干燥Cl2(1分)
防止熔融的硫堵塞导管 (2分) (3) ②③①⑤④(或③②①⑤④) (3分)
(4) 碱石灰(1分) 吸收Cl2尾气,防止空气中的水汽使S2Cl2水解(各1分,共2分)
(5)2S2Cl2+ 2H2O=SO2↑+ 3S↓+ 4HCl (2分)
【解析】试题分析:(1)S2Cl2分子结构与H2O2相似,这说明S2Cl2分子中氯原子与硫原子之间形成1对共用电子对,硫原子与硫原子之间形成1对共用电子对,所以S2Cl2电子式为![]() ;
;
(2)由于S2Cl2遇水易水解,因此进入b中的气体必须是干燥的,因此要用浓硫酸干燥氯气,即a中盛放的试剂为浓硫酸;由于硫的熔点较低,加热容易融化,所以装置c水平放置可用来防止熔融的硫堵塞导管;
(3)由于S2Cl2的熔点为-80℃,因此加热之前先通冷凝水,使生成的S2Cl2冷却液化,最后应该先停止加热后停止通氯气,以平衡容器内外压强,防止发生危险,所以实验操作顺序为②③①⑤④(或③②①⑤④);
(4)氯气有毒需要尾气处理。另外空气中也含有水蒸气,易使S2Cl2水解,所以F装置中盛放碱石灰,可以吸收Cl2尾气,防止污染环境,同时防止空气中的水蒸气加入e中使S2Cl2水解;
(5)S2Cl2水解时,只有一种元素的化合价发生了变化,由于分子氯元素的化合价处于最低价-1价,因此该元素不可能是氯元素。S元素的化合价是+1价,所以是S元素自身的氧化还原反应。又因为被氧化和被还原的该元素的物质的量之比为1:3,则根据电子得失守恒可知,被氧化的硫元素升高到+4价,而被还原的S元素降低到0价,则该反应的化学方程式为2S2Cl2+ 2H2O=SO2↑+ 3S↓+ 4HCl。

【题目】下列除杂(括号内是杂质)所选用的试剂及操作方法均正确的一组是( )
选项 | 待提纯的物质 | 选用的试剂 | 操作方法 |
A | CO2(HCl) | 饱和NaHCO3溶液 | 洗气 |
B | Mg(Al) | 过量稀盐酸 | 过滤 |
C | FeCl2溶液(FeCl3) | 足量Fe粉 | 过滤 |
D | CO2(CO) | O2 | 点燃 |
A.A
B.B
C.C
D.D
【题目】对甲、乙、丙三种衣料做纤维检验,结果如下:
方法 | 甲衣料 | 乙衣料 | 丙衣料 |
靠近火焰 | 稍微缩小 | 无变化 | 尖端熔成小球 |
燃烧气味 | 有烧焦羽毛的气味 | 无异味 | 无异味 |
浸于3%NaOH溶液中 | 变脆 | 稍微膨胀 | 几乎无变化 |
浸于10%H2SO4溶液中 | 几乎无变化 | 变脆 | 无变化 |
下列哪一项检验结果是甲、乙、丙衣料纤维最合适的结论( )
A. 甲为棉、乙为丝、丙为涤纶
B. 甲为丝、乙为棉、丙为涤纶
C. 甲为涤纶、乙为丝、丙为棉
D. 甲为棉、乙为涤纶、丙为丝
【题目】物质溶于水的过程中通常伴随着能量的变化,下表为四种物质的溶解热(“+”表示吸热,“-”表示放热)。
化学式 | NH4NO3 | NaOH | Ba(NO3)2 | KNO3 |
溶解热(kJ/mol) | +4.13 | -26.01 | + 1.57 | +3.49 |
将等物质的话的上述物质分别加入等质量的水中,所得溶液中水的离子积常数Kw最小的是
A. NH4NO3 B. NaOH C. KNO3 D. Ba(NO3)2