题目内容
【题目】硫酸亚铁晶体(FeSO4·7H2O)在医药上作补血剂。某课外小组的同学欲测定该补血剂中铁元素的含量。实验步骤如下:
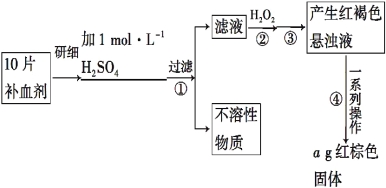
请回答下列问题:
(1)证明步骤①滤液中含有Fe2+的方法是:取样,先滴加KSCN溶液,再滴加 ,该过程的现象为______________________。
(2)步骤②加入过量H2O2的目的是 _______________________。
(3)步骤④中反应的化学方程式是 _______________________。
(4)步骤④中一系列处理的操作步骤:过滤、________、灼烧、 、称量。
【答案】(1)氯水(或双氧水、稀硝酸等合理氧化剂)溶液由浅绿色变为红色
(2)将Fe2+全部氧化为Fe3+
(3)Fe3++3OH-=Fe(OH)3↓[或Fe3++3NH3·H2O=Fe(OH)3↓+3NH4+]
(4)洗涤 冷却
【解析】
试题分析:(1)证明步骤①滤液中含有Fe2+的方法是:取样,先滴加KSCN溶液,再滴加氯水(或双氧水、稀硝酸等),若滤液由浅绿色变为红色,则说明滤液中含有Fe2+。
(2)由于H2O2具有氧化性,加入过量H2O2的目的是:将Fe2+全部氧化为Fe3+。
(3)步骤③的目的是:将Fe3+全部转化为Fe(OH)3,所以步骤③需加入过量的NaOH溶液或氨水,反应的离子方程式是Fe3++3OH-=Fe(OH)3↓[或Fe3++3NH3·H2O=Fe(OH)3↓+3NH4+]。
(4)步骤④的目的是:将产生的红褐色悬浊液分离,最终得到固体Fe2O3,所以步骤④的操作步骤是:过滤、洗涤、灼烧、冷却、称量。

练习册系列答案
 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案 黄冈创优卷系列答案
黄冈创优卷系列答案
相关题目