题目内容
化学反应原理在工业生产中具有十分重要的意义。
(1)合成氨用的氢气有多种制取方法:请你写出用C制备水煤气的化学反应方程式 。还可以由天然气或重油制取氢气:CH4+H2O(g) 高温催化剂CO+3H2;比较以上两种方法转移6mol电子时,C和CH4的质量之比是 。
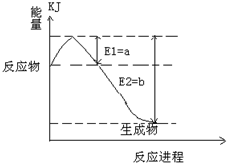
(2)工业生产可以用NH3(g)与CO2(g)经过两步反应生成尿素,两步反应的能量变化示意图如下:
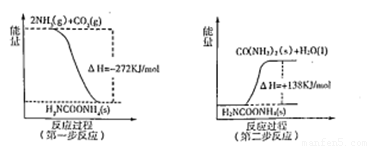
则NH3(g)与CO2(g)反应生成尿素的热化学方程式为 。
(3)已知反应Fe(s)+CO2(g)=FeO(s)+CO(g) △H=akJ/mol。测得在不同温度下,该反应的平衡常数K随温度的变化如下:
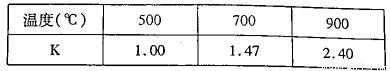
①该反应的化学平衡常数表达式K= ,a 0(填“>”、“<”或“:”)。在500℃2L密闭容器中进行反应,Fe和CO2的起始量均为4 mol,则5min后达到平街时CO2的转化率为 ,生成CO的平均速率v(CO)为 。
②700℃反应达到平衡后,要使该平衡向右移动,其他条件不变时,可以采取的措施有 (填字母)。
A.缩小反应器容积 B.增加Fe的物质的量
C.升高温度到900℃ D.使用合适的催化剂
(15分,最后一问1分,其余每空2分)(1)C+H2O(g) CO+H2;9:4
(2)2NH3(g)+CO2(g)=H2O(l)+CO(NH2)2(s) △H=-134kJ/mol
(3)①;>;50%;0.2mol/(L·min) ②C
【解析】
试题分析:(1)高温下碳和水蒸气反应生成氢气和CO,反应的化学方程式是C+H2O(g) CO+H2;反应中碳的化合价从0价升高到+2价,转移2个电子。因此转移6mol电子时,消耗碳单质的质量是:12g/mol×3mol=36g。在反应CH4+H2O(g) 高温催化剂CO+3H2中碳的化合价从-4价升高到+2价,转移6个电子。因此转移6mol电子时消耗甲烷的质量是16g,所以以上两种方法转移6mol电子时,C和CH4的质量之比是36:16=9:4。
(2)根据图像可知,第一步反应中反应物的总能量高于生成物的总能量,因此是放热反应,反应的热化学方程式是2NH3(g)+CO2(g)=H2NCOONH4(l,氨基甲酸铵) △H1=-272KJ/mol;第二步反应中,反应物的总能量低于生成物的总能量,因此反应是吸热反应,反应的化学方程式是H2NCOONH4(l)=H2O(l)+ CO(NH2)2(s) △H2=+138KJ/mol。根据盖斯定律可知,两个过程相加即得到NH3(g)与CO2(g)反应生成尿素的热化学方程式,即为2NH3(g)+CO2(g)=H2O(l)+ CO(NH2)2(s) △H=-272KJ/mol+138KJ/mol=-134kJ/mol。
(3)①化学平衡常数是在一定条件下,当可逆反应达到平衡状态时,生成物浓度的幂之积和反应物浓度的幂之积的比值,所以根据反应Fe(s)+CO2(g)=FeO(s)+CO(g)可知,该反应的平衡常数K=。由表中数据可知,对于反应①,温度越高平衡常数越大,说明升高温度平衡向正反应方向移动。由于升高温度平衡向吸热反应方向进行,故a>0。令平衡时参加反应的二氧化碳的物质的量浓度为xmol,则:
Fe(s)+CO2(g)=FeO(s)+CO(g)
起始浓度(mol/L) 2 0
转化量(mol/L) x x
平衡量(mol/L) 2-x x
所以根据平衡常数的表达式可知=1,解得x=1,所以二氧化碳的转化率为×100%=50%。其中CO表示的平均速率v(CO)==0.2mol/(L•min)。
②A、反应前后体积不变,缩小反应器容积,压强增大,化学平衡不移动,故A错误;
B、铁是固体,增加Fe的物质的量,不会引起化学平衡的移动,故B错误;
C、正方应是吸热反应,升高温度到900℃,化学平衡正向移动,故C正确;
D、催化剂只能改变反应速率,不能改变平衡状态,所以使用合适的催化剂,不会引起化学平衡的移动,故D错误,答案选C。
考点:考查氧化还原反应方程式的书写和计算;热化学方程式的书写;化学平衡常数的有关应用和计算;外界条件对平衡状态的影响等

 阅读快车系列答案
阅读快车系列答案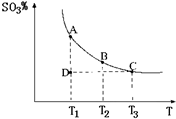 (2011?松江区模拟)运用化学反应原理研究氮、硫、氯、碘等单质及其化合物的反应有重要意义.
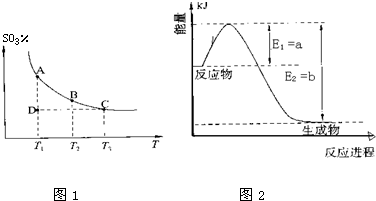
(2011?松江区模拟)运用化学反应原理研究氮、硫、氯、碘等单质及其化合物的反应有重要意义. 2SO3(g),混合体系中SO3的百分含量和温度的关系如图所示(曲线上任何一点都表示平衡状态).根据图示回答下列问题:
2SO3(g),混合体系中SO3的百分含量和温度的关系如图所示(曲线上任何一点都表示平衡状态).根据图示回答下列问题: