题目内容
将6g不纯锌(含杂质M)和6g不纯铁(含杂质N),分别加入到足量的稀硫酸中,反应到不再有氢气放出时,得到氢气的质量都是0.2g。则M、N可能是( )
| A.M为Mg,N为Cu | B.M为Fe,N为Al |
| C.M为Al,N为Na | D.N为Cu,N为Zn |
A
考点:
分析:根据金属活动顺序镁>铝>锌>铁>氢>铜,铜不能与酸反应放出氢气;若金属中混有铜,则产生氢气量会偏小;
金属与酸完全反应放出氢气的质量可利用经验推导公式“氢气质量= ×金属质量”求得;
×金属质量”求得;
使用以上方法,对金属中杂质甲、乙进行推断.
解答:解:根据金属完全反应放出氢气质量的计算公式:氢气质量= ×金属质量6g锌完全反应放出氢气的质量=
×金属质量6g锌完全反应放出氢气的质量= ×6g≈0.18g<0.2g,则该锌粉中的M应该是能与酸反应放出氢气的金属,且同等质量的金属甲完全反应产生氢气质量大于锌;而D选项中铜不能与酸反应产生氢气,故D不正确;而等质量的铁、铝、镁与酸完全反应放出氢气的质量都比锌大,因此,A、B、C选项都有可能是正确的;
×6g≈0.18g<0.2g,则该锌粉中的M应该是能与酸反应放出氢气的金属,且同等质量的金属甲完全反应产生氢气质量大于锌;而D选项中铜不能与酸反应产生氢气,故D不正确;而等质量的铁、铝、镁与酸完全反应放出氢气的质量都比锌大,因此,A、B、C选项都有可能是正确的;
6g铁与酸完全反应放出氢气的质量= ×6g≈0.21g>0.2g,则铁粉中金属N不能与酸反应或虽是能与酸反应放出氢气但等质量的金属N完全反应放出氢气的质量小于铁;而选项B中等质量的铝完全反应放出氢气的质量大于铁,故B选项不正确;
×6g≈0.21g>0.2g,则铁粉中金属N不能与酸反应或虽是能与酸反应放出氢气但等质量的金属N完全反应放出氢气的质量小于铁;而选项B中等质量的铝完全反应放出氢气的质量大于铁,故B选项不正确;
故选A.
分析:根据金属活动顺序镁>铝>锌>铁>氢>铜,铜不能与酸反应放出氢气;若金属中混有铜,则产生氢气量会偏小;
金属与酸完全反应放出氢气的质量可利用经验推导公式“氢气质量=
 ×金属质量”求得;
×金属质量”求得;使用以上方法,对金属中杂质甲、乙进行推断.
解答:解:根据金属完全反应放出氢气质量的计算公式:氢气质量=
 ×金属质量6g锌完全反应放出氢气的质量=
×金属质量6g锌完全反应放出氢气的质量= ×6g≈0.18g<0.2g,则该锌粉中的M应该是能与酸反应放出氢气的金属,且同等质量的金属甲完全反应产生氢气质量大于锌;而D选项中铜不能与酸反应产生氢气,故D不正确;而等质量的铁、铝、镁与酸完全反应放出氢气的质量都比锌大,因此,A、B、C选项都有可能是正确的;
×6g≈0.18g<0.2g,则该锌粉中的M应该是能与酸反应放出氢气的金属,且同等质量的金属甲完全反应产生氢气质量大于锌;而D选项中铜不能与酸反应产生氢气,故D不正确;而等质量的铁、铝、镁与酸完全反应放出氢气的质量都比锌大,因此,A、B、C选项都有可能是正确的;6g铁与酸完全反应放出氢气的质量=
 ×6g≈0.21g>0.2g,则铁粉中金属N不能与酸反应或虽是能与酸反应放出氢气但等质量的金属N完全反应放出氢气的质量小于铁;而选项B中等质量的铝完全反应放出氢气的质量大于铁,故B选项不正确;
×6g≈0.21g>0.2g,则铁粉中金属N不能与酸反应或虽是能与酸反应放出氢气但等质量的金属N完全反应放出氢气的质量小于铁;而选项B中等质量的铝完全反应放出氢气的质量大于铁,故B选项不正确;故选A.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
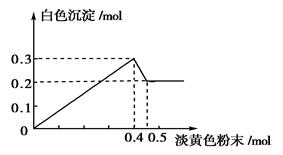
 、NH4+,加入一种淡黄色粉末固体时,加热有刺激性气味的混合气体放出,同时生成白色沉淀。当加入0.4 mol淡黄色粉末时,产生气体0.3 mol,继续加入淡黄色粉末时,产生无刺激性气味的气体,且加入淡黄色粉末时产生白色沉淀的量如下图所示。
、NH4+,加入一种淡黄色粉末固体时,加热有刺激性气味的混合气体放出,同时生成白色沉淀。当加入0.4 mol淡黄色粉末时,产生气体0.3 mol,继续加入淡黄色粉末时,产生无刺激性气味的气体,且加入淡黄色粉末时产生白色沉淀的量如下图所示。