题目内容
A、B、C、D四种元素位于短周期内,它们的原子序数依次递增。A原子核内仅有1个质子,B原子的电子总数与D原子最外层电子数相等,A原子与B原子最外层电子数之和与C原子的最外层电子数相等,D原子与B原子电子总数之和是C原子电子总数的2倍。D原子最外层电子数是其电子层数的3倍。由此推断:
(1)A、B、C、D各为什么元素?
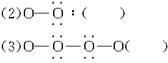
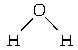
(2)A与D形成的化合物中,含有非极性键的是________,其电子式为________。
(3)BD2的电子式:________。
(1)A、B、C、D各为什么元素?
(2)A与D形成的化合物中,含有非极性键的是________,其电子式为________。
(3)BD2的电子式:________。
(1)H C N O
(2)H2O2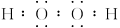
(3)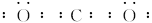
(2)H2O2
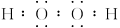
(3)
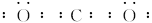
因为A原子核内仅有1个质子,所以A为H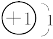 ;D原子最外层电子数是电子层数的3倍,只能为O
;D原子最外层电子数是电子层数的3倍,只能为O ;B原子的电子总数与D原子最外层电子数相等,B为C
;B原子的电子总数与D原子最外层电子数相等,B为C ;A原子与B原子最外层电子数之和与C最外层电子数相等,C为N
;A原子与B原子最外层电子数之和与C最外层电子数相等,C为N 。
。
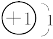 ;D原子最外层电子数是电子层数的3倍,只能为O
;D原子最外层电子数是电子层数的3倍,只能为O ;B原子的电子总数与D原子最外层电子数相等,B为C
;B原子的电子总数与D原子最外层电子数相等,B为C ;A原子与B原子最外层电子数之和与C最外层电子数相等,C为N
;A原子与B原子最外层电子数之和与C最外层电子数相等,C为N 。
。
练习册系列答案
相关题目
 同一主族。X、A、B、C、D、E、F、G均为常见的化合物,其中A和X的摩尔质量相同,A、G的焰色反应为黄色。在一定条件下,各物质相互转化关系如右图。请回答:
同一主族。X、A、B、C、D、E、F、G均为常见的化合物,其中A和X的摩尔质量相同,A、G的焰色反应为黄色。在一定条件下,各物质相互转化关系如右图。请回答: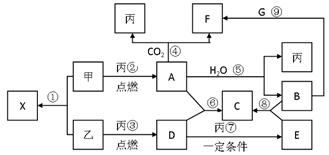
 应中,不属于氧化还原反应的是(填序号)____________________。
应中,不属于氧化还原反应的是(填序号)____________________。 后,溶液中的溶质及其物质的量分别为 ;若同体积的气体D通入100mL 2.5mo
后,溶液中的溶质及其物质的量分别为 ;若同体积的气体D通入100mL 2.5mo l·L-1的B溶液中,完全吸收后,溶液中所含离子的物质的量浓度由大到小的顺序为 。
l·L-1的B溶液中,完全吸收后,溶液中所含离子的物质的量浓度由大到小的顺序为 。