题目内容
【题目】配离子的稳定性可用K不稳衡量,例如[Ag(NH3)2]+的K不稳=![]() 。在一定温度下,向0.1mol/L硝酸银溶液中滴入稀氨水,发生反应Ag++2NH3
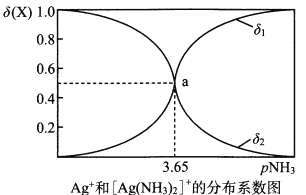
。在一定温度下,向0.1mol/L硝酸银溶液中滴入稀氨水,发生反应Ag++2NH3![]() [Ag(NH3)2]+。溶液中pNH3与δ(X)的关系如图其中pNH3=-1g[c(NH3)]、δ(X)=
[Ag(NH3)2]+。溶液中pNH3与δ(X)的关系如图其中pNH3=-1g[c(NH3)]、δ(X)= ![]() (X代表Ag+或[Ag(NH3)2]+)。下列说法正确的是
(X代表Ag+或[Ag(NH3)2]+)。下列说法正确的是
A. 图中δ1代表的是δ([Ag(NH3)2]+) B. 向溶液中滴入稀硝酸,δ(Ag+)减小
C. 该溶液中c(NH4+)+c(H+)=c(OH-) D. 该温度时,K不稳([Ag(NH3)2]+)=107.3
【答案】C
【解析】
A.pNH3越大即c(NH3)越小,则c(Ag+ )/c([Ag(NH3)2]+)越大,δ(Ag+)= ![]() 越大,故δ1代表的是δ(Ag+ ),故A选项错误;B.向体系中滴入硝酸,c(NH3)减小、δ(Ag+ )增大,故B选项错误;C.溶液电荷守恒c(Ag+)+c([Ag(NH3)2]+)+c(NH4+ )+c(H+ )=c(OH- )+c(NO3-)、物料守恒c(Ag+)+c([Ag(NH3)2]+) = c(NO3-),两式整理得c(NH4+ )+c(H+ )=c(OH- ),故C选项正确;D.选取a点即δ(Ag+ )=δ([Ag(NH3)2] ), K不稳=
越大,故δ1代表的是δ(Ag+ ),故A选项错误;B.向体系中滴入硝酸,c(NH3)减小、δ(Ag+ )增大,故B选项错误;C.溶液电荷守恒c(Ag+)+c([Ag(NH3)2]+)+c(NH4+ )+c(H+ )=c(OH- )+c(NO3-)、物料守恒c(Ag+)+c([Ag(NH3)2]+) = c(NO3-),两式整理得c(NH4+ )+c(H+ )=c(OH- ),故C选项正确;D.选取a点即δ(Ag+ )=δ([Ag(NH3)2] ), K不稳=![]() =(10-3.65)2=10-7.3,故D选项错误;答案:C。
=(10-3.65)2=10-7.3,故D选项错误;答案:C。

【题目】下列实验方案能达到相应实验目的的是
选项 | 实验目的 | 实验方案 |
A | 检验蔗糖水解生成葡萄糖 | 取适量蔗糖溶于盛有蒸馏水的试管中,滴入稀硫酸加热一段时间,冷却,滴入新制氢氧化铜悬浊液,加热至沸腾,观察有无砖红色沉淀 |
B | 实验室制备氢氧化铁胶体 | 向盛有25mL蒸馏水的烧杯中滴入5-6滴氯化铁饱和溶液,加热煮沸至溶液呈红褐色,停止加热 |
C | 比较AgCl、AgI的Ksp大小 | 向盛有10滴0.1mol/LAgNO3 溶液的试管中滴加0.1mol/LNaCl溶液至不再有沉淀生成,再滴加0.1mol/lKI溶液 |
D | 比较Mg、Al的金属性强弱 | 用导线连接镁和铝片,插入盛有氢氧化钠溶液的烧杯中,观察气泡 |
A. A B. B C. C D. D