题目内容
往浅绿色的Fe(NO3)2溶液中逐滴加入稀盐酸,溶液的颜色变化应该是( )
| A.颜色变浅 | B.逐渐加深 | C.没有改变 | D.变成绿色 |
B
因为H+、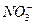 会逐渐氧化Fe2+成为Fe3+,选B。
会逐渐氧化Fe2+成为Fe3+,选B。
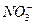 会逐渐氧化Fe2+成为Fe3+,选B。
会逐渐氧化Fe2+成为Fe3+,选B。
练习册系列答案
 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案
相关题目
题目内容
| A.颜色变浅 | B.逐渐加深 | C.没有改变 | D.变成绿色 |
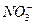 会逐渐氧化Fe2+成为Fe3+,选B。
会逐渐氧化Fe2+成为Fe3+,选B。
 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案