题目内容
 如图所示装置中,a.b都是惰性电极,通电一段时间后,b极附近溶液呈红色,此时CuSO4溶液的体积为100mL,则下列说法正确的是( )
如图所示装置中,a.b都是惰性电极,通电一段时间后,b极附近溶液呈红色,此时CuSO4溶液的体积为100mL,则下列说法正确的是( )分析:通电电解氯化钠溶液时,b极附近溶液呈红色,说明b连接的Y为电源的负极,则X为正极,电解硫酸铜时,阳极上会产生氧气,阴极上会产生金属铜,根据电解方程式确定溶液pH的变化.
解答:解:A、通电电解氯化钠溶液时,b极附近溶液呈红色,说明b连接的Y为电源的负极,则X为正极,当b电极上产生标况下气体11.2L为氢气,2H++2e-=H2↑,转移电子物质的量为1mol;依据电子守恒得到,电解硫酸铜溶液,Pt为阳极,氢氧根离子在电极上是电子发生氧化反应,4OH--4e-=2H2O+O2↑,氢氧离子减少1mol,氢原子氢离子浓度增大1mol,所以氢离子浓度为10mol/L,CuSO4溶液的PH为1,故A正确;
B、通电电解硫酸铜时,总反应为:2CuSO4+2H2O
2Cu+2H2SO4+O2↑,溶液的pH减小,故B错误;
C、通电电解硫酸铜时,X为正极,y是负极,总反应为:2CuSO4+2H2O
2Cu+2H2SO4+O2↑,溶液的pH减小,故C错误;
D、x是正极,y是负极,通电电解硫酸铜时,总反应为:2CuSO4+2H2O
2Cu+2H2SO4+O2↑,溶液的pH减小,故D错误.
故选A.
B、通电电解硫酸铜时,总反应为:2CuSO4+2H2O
| ||
C、通电电解硫酸铜时,X为正极,y是负极,总反应为:2CuSO4+2H2O
| ||
D、x是正极,y是负极,通电电解硫酸铜时,总反应为:2CuSO4+2H2O
| ||
故选A.
点评:本题考查电解池的工作原理知识,题目难度中等,注意根据电极现象判断电源的正负极为解答该题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
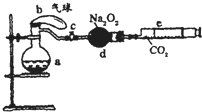 (2008?开封一模)如图所示装置中:a是盛有标准状况下的空气(氧气占
(2008?开封一模)如图所示装置中:a是盛有标准状况下的空气(氧气占 (2011?浙江五校高三联考)CuI是一种不溶于水的白色固体,它可以由反应:2Cu2++4I-═2CuI↓+I2而得到.如图所示装置中,a、b都是惰性电极,通电一段时间后,在淀粉-KI溶液中阳极周围变蓝色,则下列说法正确的是( )
(2011?浙江五校高三联考)CuI是一种不溶于水的白色固体,它可以由反应:2Cu2++4I-═2CuI↓+I2而得到.如图所示装置中,a、b都是惰性电极,通电一段时间后,在淀粉-KI溶液中阳极周围变蓝色,则下列说法正确的是( ) 如图所示装置中,a、b都是惰性电极,通电一段时间后,b极附近呈蓝色.下列说法正确的是( )
如图所示装置中,a、b都是惰性电极,通电一段时间后,b极附近呈蓝色.下列说法正确的是( ) 如图所示装置中,a、b、c、d、e、f均为惰性电极,电解质溶液均足量.接通电源后,d极附 近显红色.下列说法正确的是( )
如图所示装置中,a、b、c、d、e、f均为惰性电极,电解质溶液均足量.接通电源后,d极附 近显红色.下列说法正确的是( )