题目内容
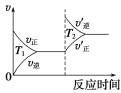
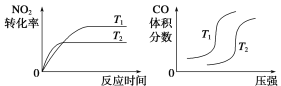
【题目】汽车尾气中CO、NO2气体在一定条件下可以发生反应:4CO(g)+2NO2(g)![]() 4CO2(g)+N2(g) ΔH=-1200 kJ·mol-1,温度不同(T2>T1)、其他条件相同时,下列图像正确的是
4CO2(g)+N2(g) ΔH=-1200 kJ·mol-1,温度不同(T2>T1)、其他条件相同时,下列图像正确的是

A B C D
【答案】B
【解析】
试题分析:A.升高温度,化学平衡逆向移动,化学反应速率会迅速增大,会离开原来的速率点,故A错误;B.升高温度,化学反应速率会迅速增大,所以T2时先达到化学平衡状态,并且化学平衡逆向移动,二氧化氮的转化率减小,故B正确;C.对于反应:4CO(g)+2NO2(g)4CO2(g)+N2(g),T不变,增大压强,平衡正向移动,一氧化碳的体积分数会减小,故C错误;D.升高温度,化学平衡逆向移动,CO的转化率减小,故D错误;故选B。

练习册系列答案
 课课练江苏系列答案
课课练江苏系列答案 名牌中学课时作业系列答案
名牌中学课时作业系列答案
相关题目