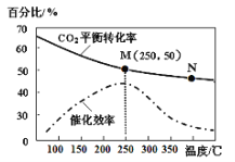
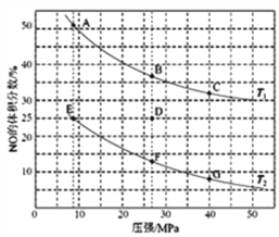
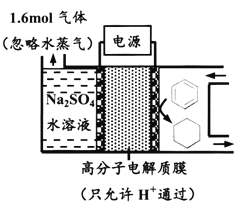
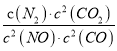题目内容
【题目】现有下列4种物质:① NH3 ②浓硝酸 ③ 浓硫酸 ④ NO。其中,遇空气迅速变成红棕色的气体是____(填序号,下同),能使湿润的红色石蕊试纸变蓝的气体是____,加入蔗糖产生“黑面包”现象的溶液是____,常温下,能用铁制容器盛放的溶液是____。
【答案】④ ① ③ ②③
【解析】
④NO遇空气迅速被氧气氧化为NO2变成红棕色的气体;①NH3易溶于水,可与水反应生成一水合氨,其水溶液显碱性,能使湿润的红色石蕊试纸变蓝;③浓硫酸具有脱水性,加入蔗糖产生“黑面包”现象;②浓硝酸和③浓硫酸都具有强氧化性,常温下,都能使铁发生钝化,则二者常温下都能用铁制容器盛放。

【题目】氯化亚铜是一种重要的化工原料,广泛应用于有机合成、石油、油脂、染料等工业。一种利用低品位铜矿(Cu2S、CuS及FeO和Fe2O3等)为原料制取CuCl的工艺流程如下:
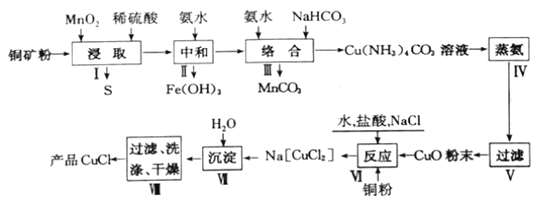
回答下列问题:
(1)步骤Ⅰ“浸取”前需将铜矿粉碎的目的是______;“浸取”时,被氧化的元素有___(填元素符号)。
(2)已知Cu2+、Mn2+、Fe3+开始生成沉淀和沉淀完全的pH如下表,则步骤Ⅱ“中和”时,pH应控制的范围为_______________;
物质 | Cu(OH)2 | Mn(OH)2 | Fe(OH)3 |
开始沉淀pH | 4.7 | 8.3 | 1.2 |
完全沉淀pH | 6.7 | 9.8 | 3.2 |
已知25℃时Ksp(MnCO3)=2.4×10—11、离子浓度为1.0×10-5mol/L时即完全沉淀,步骤Ⅲ中Mn2+完全沉淀时c(CO32—)= ________________。
(3)步骤IV加热“蒸氨”时发生反应的化学方程式为________________。
(4)步骤VI反应的离子方程式为______________,其中盐酸需过量,其原因是________________。
(5)步骤Ⅶ获得CuCl晶体需经过滤、洗涤、干燥。洗涤时,常有无水乙醇代替蒸馏水做洗涤剂的优点是______________(写一点)。