��Ŀ����
��֪���Ϊ2L�ĺ����ܱ������з�����Ӧ�� ������ݻ�ѧ��Ӧ���й�ԭ��ͬ����������
������ݻ�ѧ��Ӧ���й�ԭ��ͬ����������
��1��һ�������£�����2 mol SO2��g����2 mol O2��g����20 s���SO2������ٷֺ���Ϊ12��5%������SO2��ʾ�÷�Ӧ����20s�ڵķ�Ӧ����Ϊ____����ʱ�����ܱ������ڻ�������ѹǿ�Ƿ�Ӧǰ��____����
��2���������������Ϊ�жϣ�1���п��淴Ӧ�ﵽƽ��״̬���ݵ��ǣ�����ţ�____��
��
�ڻ��������ܶȲ���
�ۻ�������ƽ����Է�����������
�ܸ������Ũ�ȶ����ٷ����仯
��3����ͼ��ʾ�÷�Ӧ�����ʣ�v����ʱ�䣨t���ı仯�Ĺ�ϵ�������в�ͬʱ����У�SO3�İٷֺ�����ߵ��ǣ� ��


��ͼ����������Ϊt3ʱ�ı��������������� ��
t6ʱ���������������ϵ�г�������SO3���ٴ�ƽ���
SO2������ٷֺ�����t6ʱ �����\��С�����ڡ�����
��4����ͼ��P�ǿ�����ƽ�л����Ļ���������ͬ�¶�ʱ����A�����г���4 mol SO3��g�����ر�K����B�����г���2 mol SO3��g�����������ֱ�����Ӧ��

��֪��ʼʱ����A��B�������ΪaL���Իش�
�ٷ�Ӧ�ﵽƽ��ʱ����B�����Ϊ1��2a L������B��SO3ת
����Ϊ____
������K��һ��ʱ������´ﵽƽ�⣬����B�����Ϊ __L����ͨ��������������Բ��ƣ��Ҳ������¶ȵ�Ӱ�죩��
��5����֪�������ȼ����Ϊ��H=-296kJ/mol�����ⶨ��S��s������120gSO3��g���ɷ���592��5kJ����д��SO2��g����������SO3��g�����Ȼ�ѧ����ʽ____��
 ������ݻ�ѧ��Ӧ���й�ԭ��ͬ����������
������ݻ�ѧ��Ӧ���й�ԭ��ͬ������������1��һ�������£�����2 mol SO2��g����2 mol O2��g����20 s���SO2������ٷֺ���Ϊ12��5%������SO2��ʾ�÷�Ӧ����20s�ڵķ�Ӧ����Ϊ____����ʱ�����ܱ������ڻ�������ѹǿ�Ƿ�Ӧǰ��____����
��2���������������Ϊ�жϣ�1���п��淴Ӧ�ﵽƽ��״̬���ݵ��ǣ�����ţ�____��
��

�ڻ��������ܶȲ���
�ۻ�������ƽ����Է�����������
�ܸ������Ũ�ȶ����ٷ����仯
��3����ͼ��ʾ�÷�Ӧ�����ʣ�v����ʱ�䣨t���ı仯�Ĺ�ϵ�������в�ͬʱ����У�SO3�İٷֺ�����ߵ��ǣ� ��


��ͼ����������Ϊt3ʱ�ı��������������� ��
t6ʱ���������������ϵ�г�������SO3���ٴ�ƽ���
SO2������ٷֺ�����t6ʱ �����\��С�����ڡ�����
��4����ͼ��P�ǿ�����ƽ�л����Ļ���������ͬ�¶�ʱ����A�����г���4 mol SO3��g�����ر�K����B�����г���2 mol SO3��g�����������ֱ�����Ӧ��

��֪��ʼʱ����A��B�������ΪaL���Իش�
�ٷ�Ӧ�ﵽƽ��ʱ����B�����Ϊ1��2a L������B��SO3ת
����Ϊ____
������K��һ��ʱ������´ﵽƽ�⣬����B�����Ϊ __L����ͨ��������������Բ��ƣ��Ҳ������¶ȵ�Ӱ�죩��
��5����֪�������ȼ����Ϊ��H=-296kJ/mol�����ⶨ��S��s������120gSO3��g���ɷ���592��5kJ����д��SO2��g����������SO3��g�����Ȼ�ѧ����ʽ____��
��1��0.04mol/(L��s)(2��) 0.8��(2��)
��2���ۢ�(2��)
��3��A(1��) �������(1��) С(1��)
��4��40�G(2��) 2.6a(2��)
��5��2SO2 (g) + O2 (g) 2SO3 (g)����H�� ��198 kJ��mol-1(2��)
2SO3 (g)����H�� ��198 kJ��mol-1(2��)
���ߣ� SO2 (g) +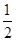 O2 (g)
O2 (g)  SO3 (g)����H�� ��99 kJ��mol-1
SO3 (g)����H�� ��99 kJ��mol-1
��2���ۢ�(2��)
��3��A(1��) �������(1��) С(1��)
��4��40�G(2��) 2.6a(2��)
��5��2SO2 (g) + O2 (g)
 2SO3 (g)����H�� ��198 kJ��mol-1(2��)
2SO3 (g)����H�� ��198 kJ��mol-1(2��)���ߣ� SO2 (g) +
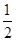 O2 (g)
O2 (g)  SO3 (g)����H�� ��99 kJ��mol-1
SO3 (g)����H�� ��99 kJ��mol-1��1�����������2SO2 + O2
 2SO3��
2SO3��ʼ�� 2mol 2mol 0 mol
���� 2xmol xmol 2xmol
ƽ�� (2-2x) mol (2-x) mol 2xmol
��������
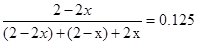 ��֮�ã�x=0.8mol
��֮�ã�x=0.8mol������SO2��ʾ�÷�Ӧ����20s�ڵķ�Ӧ����Ϊ��
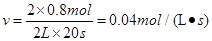
���ݰ����ӵ����ɵ����ۣ�ͬ��ͬ��������£����ʵ���֮�ȵ���ѹǿ֮�ȣ��У�
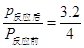 ��˷�Ӧ���ѹǿΪ��Ӧǰ��0.8����
��˷�Ӧ���ѹǿΪ��Ӧǰ��0.8������2���������ֹ�ϵ�������Ӧ���Dz����Ƿ�ﵽƽ��״̬һֱ���ڣ�����ȷ�����л��������ܶ�Ҳ��ʱ�̲���ģ���Ϊ��Ӧǰ�������壬�����غ㣬��������ǹ̶��ġ�����ȷ���۸÷�Ӧǰ������һ���������������������ʵ�����С�ķ���������Ǵﵽƽ���һ����Ҫ��־����ȷ���ܸ������Ũ�Ȳ��ٱ仯ʱ����ζ�Ÿ����Ũ��t1��һ��ֵ����ȷ��
��3��t1��t2ƽ�������ƶ���t3��t4ƽ�ⲻ�ƶ�t4 ��t5ƽ�������ƶ������ѡA
t3��t4���淴Ӧ����ͬ�ȳ̶ȸı䣬���÷�Ӧǰ��������ı䣬ֻ���Ǽ��������
�������ʱ�����������SO3���൱������ѹǿ��ƽ�������ƶ���
��4�������������2SO3
 2SO2 + O2 ��
2SO2 + O2 ��ʼ�� 2mol 0 mol 0 mol
���� 2x mol 2x mol x mol
ƽ�� (2-2x) mol (0+2x) mol L (0+x) mol
���ݰ����ӵ����ɵ����ۣ�ͬ��ͬѹ�����£����ʵ���֮�ȵ������֮�ȣ��У�
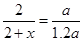 ��֮�ã�x=0.4 ����ת����Ϊ40�G
��֮�ã�x=0.4 ����ת����Ϊ40�G������K��A��B�ͳ���һ������������ٴδﵽƽ��ʱ�������Ӧ��Ϊ3��1.2aL=3.6aL����ȥA��ԭ����1L��B�������Ӧ����2.6aL��
��5�� �������У�1 mol��S��������1 mol��SO3��ų�592.5/1.5=395 kJ���������ٸ�駸�˹���ɿ�֪1 mol��SO2��g����������1 mol��SO3��g���ܷų�444-395="99" kJ����������ˣ�
2SO2 (g) + O2 (g)
 2SO3 (g)����H�� ��198 kJ��mol-1
2SO3 (g)����H�� ��198 kJ��mol-1���ߣ�SO2 (g) +
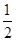 O2 (g)
O2 (g)  SO3 (g)����H�� ��99 kJ��mol-1
SO3 (g)����H�� ��99 kJ��mol-1
��ϰ��ϵ�д�
 ����ȫ���ִʾ��ƪ��ϵ�д�
����ȫ���ִʾ��ƪ��ϵ�д� �����߿����ϵ�д�
�����߿����ϵ�д�
�����Ŀ
 O2(g)=H2O(l) ��H2����285.8 kJ��mol��1
O2(g)=H2O(l) ��H2����285.8 kJ��mol��1
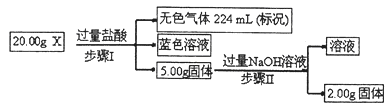

 CO(NH2)2 (l) + H2O (l)���÷�Ӧ��ƽ�ⳣ����K�����¶ȣ�T / �棩��ϵ���£�
CO(NH2)2 (l) + H2O (l)���÷�Ӧ��ƽ�ⳣ����K�����¶ȣ�T / �棩��ϵ���£� ����ͼ��1���ǰ�̼�ȣ�x����CO2ƽ��ת���ʣ������Ĺ�ϵ��������x����������ԭ���� ��
����ͼ��1���ǰ�̼�ȣ�x����CO2ƽ��ת���ʣ������Ĺ�ϵ��������x����������ԭ���� ��


 ��ʹ����ѪҺpH������7.35��7.45������ͻᷢ�����ж�����ж�����pH��c(HCO3-)��c(H2CO3)�仯��ϵ���±���
��ʹ����ѪҺpH������7.35��7.45������ͻᷢ�����ж�����ж�����pH��c(HCO3-)��c(H2CO3)�仯��ϵ���±���
 CO2(g)��H2(g)���õ������������ݣ�
CO2(g)��H2(g)���õ������������ݣ� CH3OH(g) ��H1=��116 kJ��mol��1
CH3OH(g) ��H1=��116 kJ��mol��1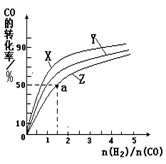

 O2(g)=CO2(g) ��H2=��283 kJ��mol��1
O2(g)=CO2(g) ��H2=��283 kJ��mol��1