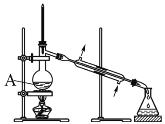
题目内容
【题目】用石墨电极完成下列电解实验,实验现象:a处试纸变蓝;b处变红,局部褪色;c处无明显变化;d处试纸变蓝。下列对实验现象的解释或推测不合理的是

A. a为电解池的阴极 B. b处有氯气生成,且与水反应生成了盐酸和次氯酸
C. c处发生了反应:Fe-3e-=Fe3+ D. d处:2H++2e-=H2↑
【答案】C
【解析】a处试纸变蓝,为阴极,有氢氧根产生,氢离子放电;b处变红,局部褪色,氯离子放电产生氯气,为阳极;c处无明显变化,铁失去电子;d处试纸变蓝,有氢氧根产生,氢离子放电,据此解答。
A.a处试纸变蓝,为阴极,生成OH-,氢离子放电,电极方程式为2H++2e-=H2↑,A正确;
B.b处变红,局部褪色,是因为氯离子放电产生氯气,氯气溶于水发生反应Cl2+H2O=HCl+HClO,HCl的酸性使溶液变红,HClO的漂白性使局部褪色,B正确;
C.Fe为c阳极,发生反应:Fe-2e- =Fe2+,C错误;
D.d处试纸变蓝,为阴极,生成OH-,氢离子放电,电极方程式为2H++2e-=H2↑,D正确;
答案为C。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
【题目】在一密闭容器中加入A、B、C三种气体,保持一定温度,在t1~t4(s) 时刻测得各物质的浓度如下表。下列结论正确的是
测定时刻/s | t1 | t2 | t3 | t4 |
c(A) / (mol·L-1) | 6 | 3 | 2 | 2 |
c(B) / (mol·L-1) | 5 | 3.5 | 3 | 3 |
c(C) / (mol·L-1) | 1 | 2.5 | 3 | 3 |
A. 在t3时刻反应已经停止
B. t3~t4内正、逆反应速率不相等
C. 在容器中发生的反应为A + B![]() C
C
D. 在t2~t3内A的平均反应速率为![]() mol·L-1·s-1
mol·L-1·s-1