题目内容
7.葡萄糖的结构简式为CH2OH-CHOH-CHOH-CHOH-CHOH-CHO,其对应的性质中不正确的是( )| A. | 与钠反应放出氢气 | B. | 可与乙酸发生酯化反应 | ||
| C. | 能发生银镜反应 | D. | 可与小苏打溶液反应,产生气泡 |
分析 CH2OH-CHOH-CHOH-CHOH-CHO中含-OH、-CHO,结合醇和醛的性质来解答.
解答 解:A.含有羟基,可与钠反应生成氢气,故A正确;
B.含有羟基,可发生酯化反应,故B正确;
C.含有醛基,可发生银镜反应,故C正确;
D.不含羧基,为非电解质,与小苏打不反应,故D错误.
故选D.
点评 本题考查有机物的官能团和性质,为高频考点,侧重于学生的分析能力的考查,题目难度不大,注意常见有机物官能团的性质.

练习册系列答案
相关题目
17.在大型演唱晚会上,观众经常使用荧光棒来增添喜庆气氛.荧光棒内草酸二苯酯和过氧化氢反应导致发光的原理大致如下:①草酸二苯酯+H2O2→C2O4+2C6H5OH;②生成的中间产物把能量传递给染料:C2O4+染料→染料*(电子激发态)+2CO2,电子激发态的染料不稳定,借发光而回到基态.下列说法不正确的是( )
| A. | 草酸二苯酯的分子式是C14H10O4 | |
| B. | 上述变化证明化学能可以转化为光能 | |
| C. | C2O4的结构简式 | |
| D. | 反应①属于酯水解反应 |
18.下列说法不正确的是( )
| A. | 氢氧燃料电池要进入广泛的实际应用,高容量储氢材料的研制是需解决的关键技术问题之一 | |
| B. | 目前科学家已经制得单原子层锗,其电子迁移率是硅的10倍,有望取代硅用于制造更好的晶体管 | |
| C. | 2013年6月航天员王亚平在太空做的水膜实验说明:水分子的组成和结构在太空中发生了改变,水才有不同于其在地球上的物理现象 | |
| D. | 元素分析仪可检验C、H、O、N、S等非金属元素,也可以检验Cr、Mn等金属元素 |
15.取某一元醇13.00g跟乙酸混合后,加入浓硫酸并加热,若反应完毕时,制得乙酸某酯15.80g,回收该一元醇1.40g.则该一元醇是( )
| A. | C7H15OH | B. | C6H13OH | C. | C5H12OH | D. | C2H5OH |
2.某药物中间体的合成路线如下.下列说法正确的是( )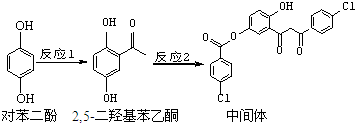

| A. | 对苯二酚在空气中能稳定存在 | |
| B. | 1 mol该中间体最多可与11 mol H2反应 | |
| C. | 2,5-二羟基苯乙酮能发生加成、水解、缩聚反应 | |
| D. | 该中间体分子中含有1个手性碳原子 |
12.下列说法错误的是( )
| A. | 等物质的量的NaX和弱酸HX混合后的溶液中c(HX)可能大于c(X-) | |
| B. | 在pH=4.5的NaHSO3溶液中,c(H2SO3)大于c(SO32-) | |
| C. | 向0.1 mol/L醋酸溶液中加水稀释的过程中c(OH-)不断增大 | |
| D. | 向含有Na2SO4的BaSO4悬浊液中加水稀释,c(Ba2+)增大 |
19.下列有关计算的分析正确的是( )
| A. | 某溶液100mL,其中含硫酸0.03mol,硝酸0.04mol,若在该溶液中投入1.92 g铜粉微热,反应后放出一氧化氮气体约为0.015mol | |
| B. | 室温时,在容积为a mL的试管中充满NO2气体,然后倒置在水中到管内水面不再上升时为止;再通入b mL O2,则管内液面又继续上升,测得试管内最后剩余气体为c mL,且该气体不能支持燃烧.则a、b的关系是a=4b+c | |
| C. | 已知某温度Ksp(Ag2S)=6×10-50,Ksp(AgCl)=2×10-6,则2AgCl(s)+S2-(aq)?Ag2S(s)+2Cl-(aq)的平衡常数约为6.7×10-37 | |
| D. | 在25℃下,将2a mol•L-1的氨水与0.02 mol•L-1的盐酸等体积混合,反应完全时溶液中c(NH4+)=c(Cl-),则用含a的代数式表示NH3•H2O的电离常数Kb=$\frac{10-9}{a-0.01}$ |
17.现有下列6组物质:①C60与金刚石②H和D③O3与18O④ 与
与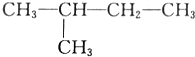 ⑤
⑤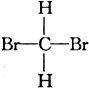 与CH2Br2⑥
与CH2Br2⑥ 与
与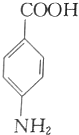
请用序号填写下表.
 与
与 ⑤
⑤ 与CH2Br2⑥
与CH2Br2⑥ 与
与
请用序号填写下表.
| 类别 | 同分异构体 | 同位素 | 同素异形体 | 同种物质 |
| 组别 |



