题目内容
短周期金属元素甲~戊在元素周期表中的相对位置如下表所示。下列判断正确的是
| A.原子半径:丙<丁<戊 | B.金属性:甲>丙 |
| C.氢氧化物碱性:丙>丁>戊 | D.最外层电子数:甲>乙 |
C
解析试题分析:A.同一周期的元素,原子序数越大,原子半径就越小。所以原子半径:丙>丁>戊,错误;B.同一主族的元素,原子核外电子层数越多,原子半径就越大,元素的金属性就越强,所以金属性:甲<丙,错误;C.同一周期的元素,原子序数越大,元素的金属性就越,其最高价的相应的碱的碱性就越弱,所以氢氧化物碱性:丙>丁>戊,正确;D.同一周期的元素,原子序数越大,原子最外层电子数就越多,所以原子最外层电子数:甲<乙,错误。
考点:考查元素的位置、结构与性质的关系的知识。

练习册系列答案
相关题目
短周期元素X、Y、Z、W的原子序数依次增大,X原子最外层电子数是其内层电子总数的3倍,Y原子最外层只有2个电子,Z单质可制成半导体材料,W与X属于同一主族。下列叙述正确的是( )
| A.元素X的简单气态氢化物的热稳定性比W弱 |
| B.元素W的最高价氧化物对应水化物的酸性比Z的弱 |
| C.化合物YX、ZX2、WX3中化学键类型相同 |
| D.原子半径的大小顺序:rY>rZ>rW>rX |
下列有关原子结构和元素周期律表述正确的是
①原子序数为15的元素的最高化合价为+3
②ⅦA族元素是同周期中非金属性最强的元素
③第二周期ⅣA族元素的原子核电荷数和中子数一定为6
④原子序数为12的元素位于元素周期表的第三周期ⅡA族
| A.①② | B.①③ | C.②④ | D.③④ |
决定元素种类的因素是( )
| A.核外电子数 | B.最外层电子数 | C.核电荷数 | D.中子数 |
a、b、c、d、e是同周期的五种元素,a和b最高价氧化物对应的水化物呈碱性,且碱性b>a,c 和d的气态氢化物的稳定性c>d;五种元素的原子得失电子后形成的简单离子中 e半径最小,下列叙述中正确的是( )
| A.原子序数关系是b <a< d< c< e | B.离子半径关系是d >c> e> b> a |
| C.原子半径关系是b> a> e> d >c | D.最外层电子数关系为c >d > a >b>e |
下列各组物质的性质及粒子的性质变化正确的是
| A.稳定性H2S>HCl>HBr>HI | B.酸性HF>HCl>HBr>HI |
| C.离子半径K+>Cl->S2->S | D.酸性HClO4>H2SO4>H2CO3>HClO |
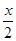 +18,N:2y+18 B.Z:
+18,N:2y+18 B.Z: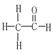 ,其一个分子中存在7对共用电子对
,其一个分子中存在7对共用电子对