题目内容
在SiO2+3C SiC+2CO↑反应中,氧化剂和还原剂的质量比为
SiC+2CO↑反应中,氧化剂和还原剂的质量比为
| A.36:30 | B.60:36 | C.2:1 | D.1:2 |
D
解析试题分析:在该反应中三份碳单质参加反应,一份作氧化剂,二份作还原剂。所以它们的质量比为:1:2.
考点:考查氧化还原反应中氧化剂、还原剂等概念的知识。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列反应中必须加入氧化剂才能进行的是( )
| A.Cl2→Cl- | B.Zn2+→Zn | C.H2→H2O | D.CuO→CuCl2 |
从海水中提取溴有如下反应:5NaBr+NaBrO3+3H2SO4=3Br2+3Na2SO4+3H2O,与上述反应在氧化还原原理上最相似的反应是
| A.2NaBr+Cl2=2NaCl+Br2 |
B.2KMnO4 K2MnO4+MnO2+O2 ↑ K2MnO4+MnO2+O2 ↑ |
| C.2H2S+SO2="3S" ↓+2H2O |
| D.2FeCl3+H2S=2FeCl2+S ↓+2HCl |
根据下列各反应,判断有关物质还原性由强到弱的顺序是( )
① H2SO3+I2+H2O = 2HI + H2SO4
② 2FeCl3+2HI=2FeCl2 + 2HCl + I2
③ 3FeCl2 + 4HNO3=2FeCl3 + NO↑ + 2H2O +Fe(NO3)3
| A.FeCl2>HI>H2SO3>NO | B.H2SO3>HI>FeCl2>NO |
| C.I2>FeCl2>H2SO3>NO | D.NO>FeCl2>H2SO3>HI |
下列粒子不具有氧化性的是
| A.ClO- | B.MnO4- | C.SO32- | D.S2- |
新型净水剂高铁酸钾(K2FeO4)为暗紫色固体,可溶于水。工业上常通过以下两步反应制备K2FeO4:①2FeCl3+10NaOH+3NaClO=2Na2FeO4+9NaCl+5H2O ②Na2FeO4 + 2KOH=K2FeO4 + 2NaOH
下列说法不正确的是
| A.反应①为氧化还原反应,反应②为复分解反应 |
| B.反应①中Na2FeO4是还原产物 |
| C.Na2FeO4 中Fe为+6价,具有强氧化性,能杀菌消毒 |
| D.若有2 mol FeCl3发生反应,转移电子的物质的量为 6 mol |
汽车剧烈碰撞时,安全气囊中发生反应: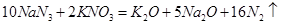 。则下列判断错误的是.
。则下列判断错误的是.
| A.该反应能在瞬间完成,并产生大量气体 |
| B.生成标准状况下2.24L气体,该反应转移电子的物质的量为0.5mol |
| C.该反应中的氧化剂为KNO3 |
| D.被氧化和被还原的N原子的物质的量之比为15:1 |
工业制ClO2的化学反应:2NaClO3+SO2+H2SO4=2ClO2+2NaHSO4,下列说法正确的是
| A.NaClO3在反应中化合价降低,失去电子 |
| B.SO2在反应中发生氧化反应 |
| C.1mol氧化剂在反应中得到2mol电子 |
| D.H2SO4 在反应中作氧化剂 |
根据下列化学方程式,判断有关物质的还原性强弱顺序正确的是
①I2+SO2+2H2O=H2SO4+2HI;②2FeCl2+Cl2=2FeCl3;③2FeCl3+2HI=2FeCl2+2HCl+I2
| A.I->Fe2+>Cl->SO2 | B.Cl->Fe2+>SO2>I- |
| C.Fe2+>I->Cl->SO2 | D.SO2>I->Fe2+>Cl- |