题目内容
【题目】化合物A由三种元素组成,是一种矿物的主要成分,可发生如下变化:
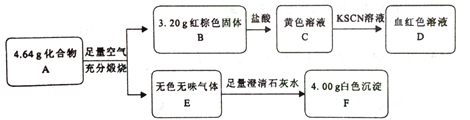
请回答:
(1) A的化学式为_____________。
(2)固体B与盐酸反应的离子方程式为____________。
(3)含化合物A的浊液长时间暴露在空气,会有部分固体表面变为红褐色,该变化的化学方程式为_________________。
【答案】 FeCO3 Fe2O3+6H+= 2Fe3++3H2O 4FeCO3+O2+6H2O= 4Fe(OH)3+4CO2
【解析】(1)根据血红色溶液D可判断3.20g红棕色固体B是氧化铁,物质的量是0.02mol;无色无味的气体E能使澄清石灰水变浑浊,说明是二氧化碳,F是碳酸钙,物质的量是0.04mol,根据碳原子守恒可知碳原子的物质的量是0.04mol,质量是0.48g,铁原子的质量是0.02mol×2×56g/mol=2.24g,因此根据原子守恒、质量守恒可知另一种元素是氧元素,质量是4.64g-2.24g-0.48g=1.92g,物质的量是0.12mol,即Fe、C、O三种原子的个数之比是1:1:3,所以A的化学式为FeCO3;(2)固体B与盐酸反应的离子方程式为Fe2O3+6H+= 2Fe3++3H2O;(3)含化合物A的浊液长时间暴露在空气,会有部分固体表面变为红褐色,说明亚铁离子被氧化为铁离子,该变化的化学方程式为4FeCO3+O2+6H2O= 4Fe(OH)3+4CO2。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目




