题目内容
写出下列物质的电离方程式:
NaCl
H2SO4
H2CO3
Al2(SO4)3
NaOH
NaCl
NaCl=Na++Cl-
NaCl=Na++Cl-
H2SO4
H2SO4=2H++SO42-
H2SO4=2H++SO42-
H2CO3
H2CO3?H++HCO3-
H2CO3?H++HCO3-
Al2(SO4)3
Al2(SO4)3=2Al3++3SO42-
Al2(SO4)3=2Al3++3SO42-
NaOH
NaOH=Na++OH-
NaOH=Na++OH-
.分析:首先判断电解质的强弱,强电解质完全电离,弱电解质部分电离,多元弱酸以第一步电离为主.
解答:解:NaCl为强电解质,完全电离,电离方程式为:NaCl=Na++Cl-;
H2SO4为强电解质,完全电离,电离方程式为:H2SO4=2H++SO42-;
H2CO3为二元弱酸,部分电离,以第一步电离为主,电离方程式为:H2CO3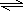 H++HCO3-;
H++HCO3-;
Al2(SO4)3为强电解质,完全电离,电离方程式为:Al2(SO4)3=2Al3++3SO42-;
NaOH为强电解质,完全电离,电离方程式为:NaOH=Na++OH-.
故答案为:NaCl=Na++Cl-;H2SO4=2H++SO42-;H2CO3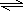 H++HCO3-;Al2(SO4)3=2Al3++3SO42-;NaOH=Na++OH-.
H++HCO3-;Al2(SO4)3=2Al3++3SO42-;NaOH=Na++OH-.
H2SO4为强电解质,完全电离,电离方程式为:H2SO4=2H++SO42-;
H2CO3为二元弱酸,部分电离,以第一步电离为主,电离方程式为:H2CO3
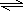 H++HCO3-;
H++HCO3-;Al2(SO4)3为强电解质,完全电离,电离方程式为:Al2(SO4)3=2Al3++3SO42-;
NaOH为强电解质,完全电离,电离方程式为:NaOH=Na++OH-.
故答案为:NaCl=Na++Cl-;H2SO4=2H++SO42-;H2CO3
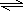 H++HCO3-;Al2(SO4)3=2Al3++3SO42-;NaOH=Na++OH-.
H++HCO3-;Al2(SO4)3=2Al3++3SO42-;NaOH=Na++OH-.点评:本题考查电离方程式的书写,题目难度不大,注意弱电解质的电离方程式的书写方法.

练习册系列答案
相关题目