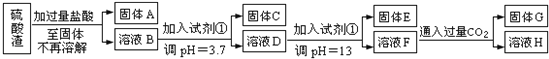
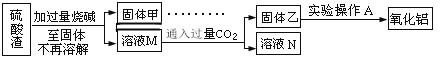
��Ŀ����
����Ŀ����ͼ�мס���Ϊ���ʣ������Ϊ�����BΪ����Һ̬�����AΪ����ɫ���壬F��G����Ԫ����ͬ�Ҿ�Ϊ�Ȼ��G��KSCN��Һ�Ժ�ɫ��
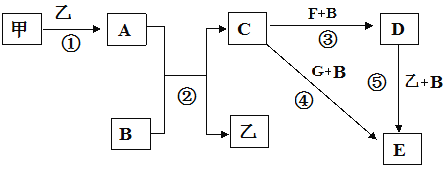
���ʴ��������⣺
��1����Ӧ��-���У�������������ԭ��Ӧ�����ڻ��Ϸ�Ӧ����______________�����������
��2����Ӧ�ݵĻ�ѧ����ʽΪ____________________________��
��3������B��Ӧ�����ӷ���ʽ _______________________________��
��4����ʵ���ҽ�C��Һ����F��Һ�У��۲쵽��������______________________��
��5����F��Һ�м�������ʵ�����A��������Ӧ���ܵ����ӷ���ʽΪ��__________________��
��6����֪����̪��c��OH���� Ϊ1.0��10��4mol/L��2.5mol/Lʱ�ʺ�ɫ���Ұ�����ڲ���ɫ����3.9g A��50g B��Ϻ����Һ�е���2�η�̪��Һ����Һ���ɫ��Ƭ�̺�ɫ��ȥ�����������Һ��������������
�ټ�ͬѧ��Ϊ����ɫѸ����ȥ����������Һ��c��OH����������ɵģ������۵��Ƿ���ȷ ��
����ͬѧ��Ϊ����ɫѸ����ȥ��������A + B = �� + H2O2 ��H2O2���������Ժ�Ư���Ե��µģ����ʵ��֤����ƿ����Һ�к�H2O2������ʵ�鷽�� ��
���𰸡�
��1���٢ݡ�
��2��4Fe��OH��2+O2+2H2O=4Fe��OH��3��
��3��2Na+2H2O=2Na++2OH-+H2����
��4��������ɫ��״������Ѹ�ٱ�Ϊ����ɫ�����ձ�Ϊ���ɫ������
��5��4Fe2++4Na2O2+6H2O=4Fe��OH��3+8Na++O2����
��6���ٷ������ƿ�ڼ�����MnO2���������������壬��֤����Һ�к�H2O2��
��������
����������ס���Ϊ���ʣ����߷�Ӧ����AΪ����ɫ���壬��AΪNa2O2���ס��ҷֱ�ΪNa�������е�һ�֣�BΪ����Һ̬�������A��Ӧ����C���ң�����֪BΪH2O����Ϊ������CΪNaOH�����ΪNa��F��G����Ԫ����ͬ�Ҿ�Ϊ�Ȼ��G��KSCN��Һ�Ժ�ɫ����GΪFeCl3��FΪFeCl2�����ת����ϵ��֪��EΪFe��OH��3��DΪFe��OH��2��
��1��������������֪����Ӧ�١����У��٢ڢ�����������ԭ��Ӧ�����л����ڻ��Ϸ�Ӧ��Ϊ�٢ݣ�
��2����Ӧ��ΪFe��OH��2������ΪFe��OH��3����Ӧ�Ļ�ѧ����ʽΪ��4Fe��OH��2+O2+2H2O = 4Fe��OH��3��
��3������ˮ��Ӧ�����ӷ���ʽΪ��2Na+2H2O=2Na++2OH-+H2����
��4���ڿ����н�NaOH��Һ����FeCl2��Һ�У���������ɫ�������������������ٱ������������ɫ�������������۲쵽�������ǣ������ɰ�ɫ������Ȼ��Ѹ�ٱ�Ϊ����ɫ�����ձ�Ϊ���ɫ��
��5����FeCl2��Һ�м�������ʵ�����Na2O2��������Ӧ���ܵ����ӷ���ʽΪ��4Fe2++4Na2O2+ 6 H2O = 4Fe��OH��3 + 8Na+ + O2����
��6����3.9g�������Ƶ����ʵ���Ϊ0.05mol�����ݷ�Ӧ2Na2O2+2H2O=4NaOH+O2����֪���������Ƶ����ʵ���Ϊ0.1mol��c��OH���� Ϊ1mol/L����̪��1.0��10��4mol/L��2.5mol/Lʱ�ʺ�ɫ���Ұ�����ڲ���ɫ������ˡ���ɫѸ����ȥ��������Ϊ��Һ��c��OH����������ɵġ�
�������H2O2������������̣�������������������ȡ��ƿ�е���Һ�����Թ��У���������MnO2�������ݷų����ô����ǵ�ľ�����飬ľ����ȼ��˵����Һ�п�����H2O2��