题目内容
【题目】关于各图的说法(其中①③④中均为惰性电极)正确的是( )
A.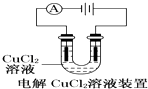
装置中阴极产生的气体能够使湿润淀粉KI试纸变蓝
B.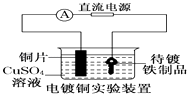
装置中待镀铁制品应与电源正极相连
C.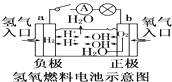
装置中电子由b极流向a极
D.
装置中的离子交换膜可以避免生成的Cl2与NaOH溶液反应
【答案】D
【解析】解:A.电解时,阴极发生还原反应,电极方程式为Cu2++2e﹣=Cu,阳极发生氧化反应,电极方程式为2Cl﹣﹣2e﹣=Cl2↑,装置中阴极不会产生气体,故A错误;
B.电镀铜电解池中,阳极上金属失电子,阴极上铜离子得电子,装置中待镀铁制品应与电源负极相连,镀件是阴极,故B错误;
C.通入氧气的一极为正极,通氢气的一电极是负极,电子由负极流向正极,由a极流向b极,故C错误;
D.装置中的离子交换膜只允许部分离子经过,两极产物氯气、氢氧化钠在隔膜的作用下,避免反应的发生,故D正确.
故选D.

 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 名校提分一卷通系列答案
名校提分一卷通系列答案 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案 新卷王期末冲刺100分系列答案
新卷王期末冲刺100分系列答案【题目】某学习小组在实验室研究SO2与Ba(NO3)2溶液的反应:
实验:向盛有2mL 0.1mol/L Ba(NO3)2溶液的试管中,缓慢通入SO2气体,试管内有白色沉淀产生,液面上方略显浅棕色.
探究1:白色沉淀产生的原因.
(1)白色沉淀是 .
(2)分析白色沉淀产生的原因,甲同学认为是NO3﹣氧化了SO2 , 乙同学认为是溶液中溶解的O2氧化了SO2 .
①支持甲同学观点的实验证据是 .
②依据甲的推断,请写出Ba(NO3)2溶液与SO2反应的离子方程式 .
(3)乙同学通过下列实验证明了自己的推测正确,请完成实验方案:
实验操作 | 实验现象 |
向2mLmol/L溶液(填化学式)中通入SO2 |
(4)探究2:在氧化SO2的过程中,NO3﹣和O2哪种微粒起到了主要作用.
实验操作 | 实验数据 |
向烧杯中加入煮沸了的0.1mol/L的BaCl2溶液25mL,再加入25mL植物油,冷却至室温,用pH传感器测定溶液pH随时间(t)的变化曲线 |
|
向烧杯中分别加入25mL 0.1mol/L的BaCl2溶液、Ba(NO3)2溶液,通入SO2 , 用pH传感器分别测定溶液pH随时间(t)变化的曲线. |
|
图1,在无氧条件下,BaCl2溶液pH下降的原因是 .
(5)图2,BaCl2溶液中发生反应的离子方程式为 .
(6)依据上述图象你得出的结论是 , 说明理由 .
【题目】分析下列氧化还原反应中化合价变化的关系,氧化剂和氧化产物都正确的是
化学反应方程式 | 氧化剂 | 氧化产物 | |
A | 3Cl2+2Fe | Fe | FeCl3 |
B | 2 Na+2 H2O===2 NaOH+H2↑ | H2O | NaOH |
C | 2HClO | HClO | HClO |
D | Cl2+Na2SO3+H2O =2HCl+Na2SO4 | Cl2 | HCl |
A. A B. B C. C D. D
【题目】下列操作与实验现象不匹配的是( )
反应 | 现象 | |
A | 把明矾溶液滴入含悬浮泥沙的水中 | 产生不溶物 |
B | 在氯气中点燃氢气 | 产生苍白色火焰 |
C | 将氯气通入紫色石蕊溶液 | 溶液最终由紫色变为红色 |
D | 向硅酸钠浓溶液中滴入稀硫酸 | 出现胶状物 |
A. A B. B C. C D. D

