题目内容
7.根据反应8NH3+3Cl2═6NH4Cl+N2,回答下列问题.(1)氧化剂Cl2,还原剂NH3
(2)用双线桥法标明电子转移的方向和数目

(3)氧化剂与氧化产物的物质的量之比3:1
(4)当生成28gN2时,被氧化的物质的质量是34g.
分析 该反应中N元素化合价由-3价变为0价、Cl元素化合价由0价变为-1价,所以NH3是还原剂、Cl2是氧化剂,反应中转移6e-,以此来解答.
解答 解:(1)该反应中N元素化合价由-3价变为0价、Cl元素化合价由0价变为-1价,所以NH3是还原剂、Cl2是氧化剂,故答案为:Cl2;NH3;
(2)反应中N元素的化合价由-3升高为0,Cl元素的化合价0降低为-1价,2molNH3作还原剂转移电子为6mol,则反应电子转移的方向和数目为 ,故答案为:
,故答案为: ;
;
(3)由反应可知,3molCl2为氧化剂,对应生成1molN2为氧化产物,则氧化剂与氧化产物的物质的量之比为3:1,故答案为:3:1;
(4)当生成28gN2时,n(N2)=$\frac{28g}{28g/mol}$=1mol,由N原子守恒可知2mol氨气被氧化,则被氧化的物质的质量是2mol×17g/mol=34g,故答案为:34.
点评 本题考查氧化还原反应及计算,为高频考点,把握反应中元素的化合价变化及基本概念为解答的关键,侧重分析、应用及计算能力的考查,题目难度不大.

练习册系列答案
相关题目
17. 为了探究AgNO3的热稳定性和氧化性,某化学兴趣小组设计了如下实验.
为了探究AgNO3的热稳定性和氧化性,某化学兴趣小组设计了如下实验.
Ⅰ.AgNO3的热稳定性
利用如图所示的实验装置,加热A中的AgNO3固体,试管A中有红棕色气体产生,B中无红棕色气体产生,在装置C中收集到无色气体.当反应结束后,测得试管中残留黑色固体Ag.(夹持及加热仪器均省略)
(1)C中集气瓶收集的气体为氧气,要收集纯净的该气体,正确的操作是等到导气管中气泡均匀放出时再收集.
(2)甲同学认为仅凭试管A中有红棕色的气体产生就判定有NO2产生是错误的,因为无色NO遇到空气也会变成红棕色,所以加热前应当排净装置中的空气,你是否同意他的观点?并说明理由:否;硝酸银分解生成氧气.
Ⅱ.AgNO3的氧化性
将光亮的铁丝伸入盛有AgNO3溶液的大试管中,一段时间后将铁丝取出.为检验溶液中Fe的氧化产物,猜测如下:
假设一:Fe被氧化成Fe2+;
假设二:Fe被氧化成Fe3+;
假设三:Fe被氧化成Fe2+或Fe3+.
已知:溶液中的Ag+能与SCN-反应,干扰实验.选用如下试剂设计一个实验验证假设三.可选用的试剂:KSCN溶液、酸性KMnO4溶液、氯水、盐酸、硝酸、NaCl溶液.完成如表:
实验结论:Fe的氧化产物为Fe2+和Fe3+.
 为了探究AgNO3的热稳定性和氧化性,某化学兴趣小组设计了如下实验.
为了探究AgNO3的热稳定性和氧化性,某化学兴趣小组设计了如下实验.Ⅰ.AgNO3的热稳定性
利用如图所示的实验装置,加热A中的AgNO3固体,试管A中有红棕色气体产生,B中无红棕色气体产生,在装置C中收集到无色气体.当反应结束后,测得试管中残留黑色固体Ag.(夹持及加热仪器均省略)
(1)C中集气瓶收集的气体为氧气,要收集纯净的该气体,正确的操作是等到导气管中气泡均匀放出时再收集.
(2)甲同学认为仅凭试管A中有红棕色的气体产生就判定有NO2产生是错误的,因为无色NO遇到空气也会变成红棕色,所以加热前应当排净装置中的空气,你是否同意他的观点?并说明理由:否;硝酸银分解生成氧气.
Ⅱ.AgNO3的氧化性
将光亮的铁丝伸入盛有AgNO3溶液的大试管中,一段时间后将铁丝取出.为检验溶液中Fe的氧化产物,猜测如下:
假设一:Fe被氧化成Fe2+;
假设二:Fe被氧化成Fe3+;
假设三:Fe被氧化成Fe2+或Fe3+.
已知:溶液中的Ag+能与SCN-反应,干扰实验.选用如下试剂设计一个实验验证假设三.可选用的试剂:KSCN溶液、酸性KMnO4溶液、氯水、盐酸、硝酸、NaCl溶液.完成如表:
| 操作 | 现象 | 结论或目的 |
| (1)取少量溶液于试管中,向溶液中加入足量NaCl溶液 | 白色沉淀 | 除尽Ag+ |
| (2)取少量上层清液于试管中,加入取少量上述溶液于试管中加入 KSCN溶液,振荡 | 溶液变血红色 | 存在Fe3+ |
| (3)取(1)中少量上层清液于试管中,加入加入 酸性KMnO4溶液,振荡 | 紫红色消失 | 存在Fe2+ |
18.下列离子方程式中,正确的是( )
| A. | 稀硫酸与氢氧化钡溶液反应:H++OH-═H2O | |
| B. | 铁与氯化铁溶液反应:Fe+2Fe3+═3Fe2+ | |
| C. | 实验室制氯气:MnO2+4HCl═Mn2++2Cl-+Cl2↑+2H2O | |
| D. | 向氯化铝溶液滴加少量氨水:Al3++3OH-═Al(OH)3↓ |
15.如图是一种合金材料储氢后的晶胞结构示意图,该晶体中X、Y、Z微粒的个数比为( )
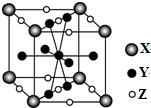

| A. | 1:1:1 | B. | 1:3:3 | C. | 4:4:5 | D. | 1:5:3 |
2.下列说法中正确的是( )
| A. | H2SO4的摩尔质量是98g | |
| B. | 标准状况下,2.24 L水的质量是1.8g | |
| C. | 16gO3比16gO2所含的氧原子数多 | |
| D. | 22g二氧化碳与标准状况下11.2L HCl含有相同的分子数 |
12.下列溶液中,溶液的物质的量浓度为1mol•L-1是( )
| A. | 将40gNaOH溶于1L水中所得的溶液 | |
| B. | 将58.5gNaCl溶于水配成1L溶液 | |
| C. | 将0.5mol•L-1氯化钠溶液100mL加热蒸发掉50g水的溶液 | |
| D. | 含K+为2mol的K2SO4溶液 |
16.NA为阿伏伽德罗常数的值,下列叙述正确的是( )
| A. | 常温常压下,2g 氢气所含原子数目为2NA | |
| B. | 36g H2O中含有的质子数为10NA | |
| C. | 标准状况下,11.2L水中含有的分子数是0.5NA | |
| D. | 1mol 氯气与足量水反应,转移的电子数是2NA |
 ;
;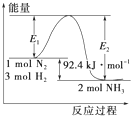 是可逆反应反应物不能完全转化.
是可逆反应反应物不能完全转化.