题目内容
现有如下几个离子方程式①CaCO3+2H+===Ca2++H2O+CO2↑②H++CO32—===HCO3— ③CO2+H2O+ClO-===HClO+HCO3— ④CO32—+HSO3—===HCO3—+SO32—,由此得出的如下结论中不正确的是( )
| A.CO32—与H+、Ca2+不能大量共存 | B.H2CO3的酸性比HClO强,比H2SO3弱 |
| C.H2SO3是一种强酸 | D.H2CO3、HClO都属于弱酸 |
C
试卷分析:根据反应①可知CO与H+、Ca2+不能大量共存。根据反应③④可知H2CO3的酸性比HClO强,比H2SO3弱。根据②③可知H2CO3、HClO都属于弱酸。根据④可知,H2SO3属于弱酸。答案选C。
点评:酸性较强可以与酸性较弱的盐溶液反应生成酸性较弱的酸和酸性较强的盐溶液。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
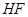 溶液加水不断稀释,下列各量始终保持增大的是( )
溶液加水不断稀释,下列各量始终保持增大的是( )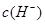
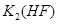
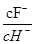
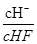
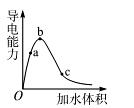
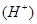 由小到大的顺序是 。
由小到大的顺序是 。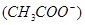 增大,c
增大,c