题目内容
11.下列对一些物质或化学反应的分类以及依据正确的是( )| A. | 豆浆是胶体,因为豆浆中的分散质粒子直径在1nm~100nm之间 | |
| B. | NaCl溶液是电解质,因为NaCl溶液能导电 | |
| C. | Na和H2O的反应不是离子反应,因为反应中没有离子参加 | |
| D. | H2SO4是酸,因为H2SO4中含有氢元素 |
分析 A.胶体分散质粒子直径在1nm~100nm之间;
B.在水溶液里或熔融状态下能导电的化合物是电解质;
C.有离子参加或生成的反应是离子反应;
D.据电离时生成的阳离子都是氢离子的化合物是酸.
解答 解:A.豆浆是胶体,因为豆浆中的分散质粒子直径在1nm~100nm之间,故A正确;
B.NaCl溶液是混合物,故B错误;
C.Na和H2O的反应是离子反应,因为反应中离子生成,故C错误;
D.H2SO4是酸,因为H2SO4电离时生成的阳离子都是氢离子,故D错误.
故选A.
点评 本题主要考查了物质的分类、离子反应的概念、胶体的概念等,难度不大,掌握分类的依据是解题的关键.

练习册系列答案
相关题目
6.下列实验操作都能够达到预期目的是( )
①用精密pH试纸测得某溶液pH为3.5
②用米汤直接检验食用盐中是否含有碘元素
③用pH试纸测定溶液的pH时,需先用蒸馏水润湿试纸
④滴入酚酞溶液确定纯碱中有无烧碱
⑤用酸式滴定管量取20.00mL高锰酸钾酸性溶液
⑥蒸干AlCl3溶液可得纯净的无水氯化铝.
①用精密pH试纸测得某溶液pH为3.5
②用米汤直接检验食用盐中是否含有碘元素
③用pH试纸测定溶液的pH时,需先用蒸馏水润湿试纸
④滴入酚酞溶液确定纯碱中有无烧碱
⑤用酸式滴定管量取20.00mL高锰酸钾酸性溶液
⑥蒸干AlCl3溶液可得纯净的无水氯化铝.
| A. | ②④⑥ | B. | ②⑥ | C. | ①⑤ | D. | ④⑤⑥ |
19.下列说法中正确的是( )
| A. | 在水电离出的c(H+)=1×10-13mol/L的溶液中下列离子一定能大量共存:Na+、CO32-、Cl-、K+ | |
| B. | 氢氧根离子浓度相同的氢氧化钠溶液和氨水导电能力相同 | |
| C. | K2SO3溶液中c(K+)与c(SO32-)之比为2:1 | |
| D. | 硫酸是强电解质,故纯硫酸能导电 |
6.下列关于σ键和π键说法正确的是( )
| A. | σ键是由两个p电子“肩并肩”重叠形成的 | |
| B. | σ键和π键都是共价键,σ键比π键更稳定 | |
| C. | 乙烯分子中的 和乙炔分子中的-C≡C-都是π键 和乙炔分子中的-C≡C-都是π键 | |
| D. | H2分子中含有σ键,HCl分子中含π键 |
16.下列说法正确的是( )
| A. | 氢气的燃烧热为△H=-285.5k•Jmol-1,则电解水的热化学方程式为2H2O(l)$\frac{\underline{\;电解\;}}{\;}$2H2(g)+O2(g)△H=+285.5k•Jmol-1 | |
| B. | 密闭容器中,9.6g硫粉与11.2g铁粉混合加热生成硫化亚铁17.6g时,放出19.12kJ热量.则Fe(s)+S(s)═FeS(s)△H=-95.6kJ•mol-1 | |
| C. | 500℃、30MPa下,将0.5molN2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g)+3H2(g)═2NH3(g)△H=-38.6k•Jmol-1 | |
| D. | 相同条件下,在两个相同的恒容密闭容器中,1molN2和3molH2反应放出的热量与2molN2和3molH2反应放出的热量一样多 |
3.由不同种类的原子组成的物质可能是( )
①纯净物
②混合物
③单质
④化合物
⑤金属
⑥非金属
⑦酸
⑧碱
⑨盐
⑩氧化物.
①纯净物
②混合物
③单质
④化合物
⑤金属
⑥非金属
⑦酸
⑧碱
⑨盐
⑩氧化物.
| A. | ①③⑤⑦⑨ | B. | ②④⑧⑩ | C. | ①③ | D. | 全部 |
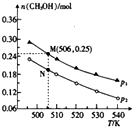 以天然气为原料合成甲醇常见的方法有水煤气法和目前正在开发的直接氧化法.
以天然气为原料合成甲醇常见的方法有水煤气法和目前正在开发的直接氧化法.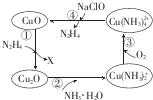 肼(N2H4)的性质类似于氨气,易溶于水,是塑料、橡胶发泡剂的原料.将肼蒸气通入Cu0胶体中,可发生如图所示的转化.
肼(N2H4)的性质类似于氨气,易溶于水,是塑料、橡胶发泡剂的原料.将肼蒸气通入Cu0胶体中,可发生如图所示的转化. .
.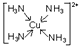 .
.