题目内容
下列叙述中,不能用平衡移动原理解释的是
| A.红棕色的NO2,加压后颜色先变深后变浅 |
| B.黄绿色的氯水光照后颜色变浅 |
| C.由H2、Br2(g)、HBr(g)气体组成的平衡体系加压后颜色变深 |
| D.工业合成氨反应中加压有利于提高氨气的产率 |
C
试题分析:A. 2NO2(红棕色)
 N2O4(无色)。加压后由于单位体积内的NO2分子数增多,所以颜色加深。增大压强,根据平衡移动原理,可逆反应向气体体积减小的方向即正反应方向移动,又使NO2的浓度又有所减小。与题目要求不符。错误。B.氯气溶于水发生反应:Cl2+H2O
N2O4(无色)。加压后由于单位体积内的NO2分子数增多,所以颜色加深。增大压强,根据平衡移动原理,可逆反应向气体体积减小的方向即正反应方向移动,又使NO2的浓度又有所减小。与题目要求不符。错误。B.氯气溶于水发生反应:Cl2+H2O H++Cl-+HClO光照发生2HClO
H++Cl-+HClO光照发生2HClO 2HCl+O2↑由于减小了生成物HClO的浓度,破坏了可逆反应的平衡,减小生成物的浓度,平衡向正反应方向移动,不断消耗氯气,使黄绿色的氯水后颜色逐渐变浅。不符合题目要求。错误。C.反应H2+Br2(g)
2HCl+O2↑由于减小了生成物HClO的浓度,破坏了可逆反应的平衡,减小生成物的浓度,平衡向正反应方向移动,不断消耗氯气,使黄绿色的氯水后颜色逐渐变浅。不符合题目要求。错误。C.反应H2+Br2(g) 2HBr(g)是应该反应前后气体体积相等的反应。当给该平衡体系加压后由于各物质的浓度都增大颜色变深。但增大压强化学平衡不发生移动。符合题意。正确。D.工业合成氨反应N2+3H2
2HBr(g)是应该反应前后气体体积相等的反应。当给该平衡体系加压后由于各物质的浓度都增大颜色变深。但增大压强化学平衡不发生移动。符合题意。正确。D.工业合成氨反应N2+3H2  2NH3的正反应是个气体体积减小的反应。增大压强,化学平衡向气体体积减小的方向即正反应方向移动。产生更多的NH3。故加压可提高NH3的产率。,不符合题意。错误。
2NH3的正反应是个气体体积减小的反应。增大压强,化学平衡向气体体积减小的方向即正反应方向移动。产生更多的NH3。故加压可提高NH3的产率。,不符合题意。错误。
练习册系列答案
相关题目
 CH3 OH(g) △H="a" kJ/mol,
CH3 OH(g) △H="a" kJ/mol, Ni(CO)4(g),已知该反应在25℃和80℃时的平衡常数分别为5×104和2,下列说法正确的是
Ni(CO)4(g),已知该反应在25℃和80℃时的平衡常数分别为5×104和2,下列说法正确的是 2C(g)
2C(g)  H=" -a" kJ/mol(a>0),在一个有催化剂的固定容积的密闭容器中加入2molA2和1molB2,在500℃是充分反应达到平衡后C的浓度为w mol/L,放出热量b kJ。
H=" -a" kJ/mol(a>0),在一个有催化剂的固定容积的密闭容器中加入2molA2和1molB2,在500℃是充分反应达到平衡后C的浓度为w mol/L,放出热量b kJ。 CO(g)+H2(g),当增加反应物物质的量时,平衡一定向正反应方向移动
CO(g)+H2(g),当增加反应物物质的量时,平衡一定向正反应方向移动
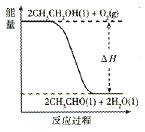
 eC(气)+fD(气),反应过程中保持其他条件不变,C的体积分
eC(气)+fD(气),反应过程中保持其他条件不变,C的体积分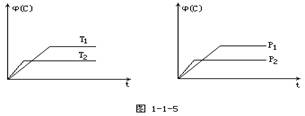
 3C(g) ΔH<0,达到平衡后,改变一个条件(x),下列量(y)一定符合图中曲线的是( )
3C(g) ΔH<0,达到平衡后,改变一个条件(x),下列量(y)一定符合图中曲线的是( ) 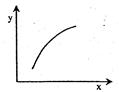
 CH3OH(g)+H2O(g) ΔH <0,容器中CH3OH的物质的量随时间变化如曲线I所示,平衡时容器内压强为P。改变某一条件重新进行上述反应,CH3OH的物质的量随时间变化如曲线II所示。下列说法正确的是
CH3OH(g)+H2O(g) ΔH <0,容器中CH3OH的物质的量随时间变化如曲线I所示,平衡时容器内压强为P。改变某一条件重新进行上述反应,CH3OH的物质的量随时间变化如曲线II所示。下列说法正确的是