题目内容
短周期元素X、Y、Z、W、R的化合价与原子序数的关系如图所示.下列说法正确的是( )


| A、原子半径:Z>Y>X |
| B、气态氢化物的稳定性:Y<R |
| C、Z和Y能形成化合物Z2Y和Z2Y2 |
| D、Z和W两者最高价氧化物对应的水化物不能相互反应 |
考点:原子结构与元素周期律的关系
专题:元素周期律与元素周期表专题
分析:由表中化合价可知,Y的化合价为-2价,没有正化合价,故Y为O元素,X的化合价为+4、-4价,处于ⅣA族,原子序数比O元素小,故X为C元素,Z的化合价为+1价,处于ⅠA族,原子序数大于O元素,故Z为Na元素,W为+3价,为Al元素,R的化合价为+6、-2价,故R为S元素.结合对应单质、化合物的性质以及题目要求解答该题.
解答:
解:由表中化合价可知,Y的化合价为-2价,没有正化合价,故Y为O元素,X的化合价为+4、-4价,处于ⅣA族,原子序数比O元素小,故X为C元素,Z的化合价为+1价,处于ⅠA族,原子序数大于O元素,故Z为Na元素,W为+3价,为Al元素,R的化合价为+6、-2价,故R为S元素.
A.同周期随原子序数增大,原子半径减小,故原子半径Li>C>O,同主族自上而下原子半径增大,故Na>Li,故Na>C>O,即Z>X>Y,故A错误;
B.非金属性O>S,即Y>R,非金属性越强氢化物越稳定,故气态氢化物的稳定性:Y>R,故B错误;
C.Z和Y形成的化合物是氧化钠、过氧化钠,分别为Na2O和Na2O2,故C正确;
D.Z和W两者最高价氧化物对应的水化物分别为氢氧化钠和氢氧化铝,其中氢氧化铝为两性氢氧化物,与氢氧化钠溶液反应,故D错误.
故选C.
A.同周期随原子序数增大,原子半径减小,故原子半径Li>C>O,同主族自上而下原子半径增大,故Na>Li,故Na>C>O,即Z>X>Y,故A错误;
B.非金属性O>S,即Y>R,非金属性越强氢化物越稳定,故气态氢化物的稳定性:Y>R,故B错误;
C.Z和Y形成的化合物是氧化钠、过氧化钠,分别为Na2O和Na2O2,故C正确;
D.Z和W两者最高价氧化物对应的水化物分别为氢氧化钠和氢氧化铝,其中氢氧化铝为两性氢氧化物,与氢氧化钠溶液反应,故D错误.
故选C.
点评:本题考查结构性质与位置关系、元素周期律等,侧重于学生的分析能力的考查,难度不大,根据推断元素是解题的关键,根据化合价结合原子序数进行推断.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列有关说法正确的是( )
| A、水中存在电离平衡,向纯水中加酸或加入碱都抑制水的电离,加盐可以促进水的电离 |
| B、将0.2mol/L的NH3?H2O与0.1mol/L的HCl溶液等体积混合,则c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
| C、常温下,0.1mol/L的NaHCO3溶液中,c(Na+)+c(H+)═c(OH-)+c(HCO3-)+2c(CO32-) |
| D、在25℃时,除去水体中的Ba2+选择Na2CO3比Na2CrO4好[已知Ksp(BaCO3)>Ksp(BaCrO4)] |
下表为部分短周期元素的原子半径及主要化合价,根据表中信息判断,下列叙述正确的是( )
| 元素代号 | X | Y | Z | M | N |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.071 | 0.099 |
| 主要化合价 | +2 | +3 | +6、-2 | -1 | -1 |
| A、X、Y最高价氧化物对应水化物的碱性:Y>X |
| B、M、N形成的简单离子的还原性:N->M- |
| C、气态氢化物的稳定性:HM<H2Z |
| D、最高价氧化物对应的水化物的酸性:H2ZO4>HNO4 |
下列叙述错误的是( )
| A、通常情况下,甲烷跟强酸、强碱、酸性 溶液都不起反应 |
| B、甲烷化学性质比较稳定,不能被任何氧化剂氧化 |
| C、甲烷跟氯气反应无论生成一氯,还是多氯,都属于取代反应 |
| D、甲烷的四种有机取代物都难溶于水 |
下列有关化学实验的说法正确的是( )
| A、除去NO气体中的NO2气体,把混合气体通过盛有水的洗气瓶 |
| B、把氯气通入石蕊试液中和把二氧化硫通入石蕊试液中的现象相同:先变红后褪色 |
| C、鉴别碳酸钠溶液和碳酸氢钠溶液可以用澄清石灰水 |
| D、工业上制取金属铝和金属镁都是电解熔融的二者的氯化物 |
下列说法中正确的是( )
A、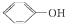 与 与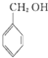 互为同系物 互为同系物 |
| B、乙醇和乙醚互为同分异构体 |
| C、可用浓溴水来区分乙醇和苯酚 |
| D、乙醇、乙二醇、丙三醇互为同系物 |
下列实验操作正确的是( )
A、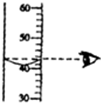 |
B、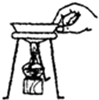 |
C、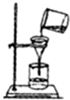 |
D、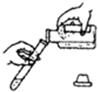 |