题目内容
【题目】向含有Fe2+、I﹣、Br﹣的溶液中通入适量氯气,溶液中各种离子的物质的量变化如图所示有关说法正确的是( ) 
A.线段BC代表Cl﹣数目的变化情况
B.原混合溶液中c(FeBr2)=6mol/L
C.当通入Cl22mol时,溶液中已发生的离子反应可表示为:2Fe2++2I﹣+2Cl2=2Fe3++I2+4 Cl﹣
D.原溶液中n(Fe2+):n(I﹣):n(Br﹣)=2:2:3
【答案】C
【解析】解:还原性为I﹣>Fe2+>Br﹣ , 则先发生2I﹣+Cl2═I2+2Cl﹣ , I﹣反应完毕再发生2Fe2++Cl2═2Fe3++2Cl﹣ , 最后发生反应2Br﹣+Cl2═Br2+2Cl﹣ , A.B点时溶液中I﹣完全反应,溶液中存在Fe2+和Br﹣ , BC段发生2Fe2++Cl2═2Fe3++2Cl﹣ , 代表Fe3+的物质的量的变化情况,而不是氯离子,故A错误;
B.由图可知,BC段发生2Fe2++Cl2═2Fe3++2Cl﹣ , Fe2+反应完毕消耗氯气2mol,由方程式可知n(Fe2+)=2×2mol=4mol,则n(FeBr2)=4mol,故B错误;
C.AB段发生2I﹣+Cl2═I2+2Cl﹣ , 2mol的I﹣消耗1mol氯气,BC段发生2Fe2++Cl2═2Fe3++2Cl﹣ , 余下的1mol氯气再与2molFe2+反应,故参加反应的n(Fe2+):n(I﹣)=1:1,故通入2molCl2时,溶液中已发生的离子反应可表示为2Fe2++2I﹣+2Cl2═2Fe3++I2+4Cl﹣ , 故C正确;
D.由图可知AB段消耗氯气1mol,发生2I﹣+Cl2═I2+2Cl﹣ , 故n(I﹣)=2n(Cl2)=2mol,BC段发生2Fe2++Cl2═2Fe3++2Cl﹣ , 消耗氯气2mol,故n(Fe2+)=2n(Cl2)=2×2mol=4mol,DE段发生2Br﹣+Cl2═Br2+2Cl﹣ , 消耗氯气3mol,故n(Br﹣)=2n(Cl2)=6mol,故原溶液中n(Fe2+):n(I﹣):n(Br﹣)=4mol:2mol:6mol=2:1:3,故D错误;
故选C.

 全优点练单元计划系列答案
全优点练单元计划系列答案【题目】实验室中某些气体的制取、收集及尾气处理装置如图所示(省略夹持、加热和净化装置).仅用此装置和表中提供的物质完成相关实验,最合理的选项是( )
选项 | a中的物质 | b中的物质 | c中收集的气体 | d中的物质 |
A | 浓硝酸 | Cu | NO2 | NaOH溶液 |
B | 浓氨水 | CaO | NH3 | H2O |
C | 稀硝酸 | Cu | NO | H2O |
D | 浓硫酸 | Cu | SO2 | 饱和NaHSO3溶液 |
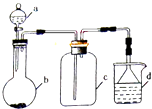
A.A
B.B
C.C
D.D
【题目】某化学兴趣小组的成员捡到一块矿石,观察外观发现该矿石坚硬且呈红褐色,投入水中没有任何变化,再向水中加浓盐酸至过量,矿石部分溶解,并有大量无色气体生成.学生猜测该矿石可能由CaCO3、SiO2、Fe2O3三种成分组成,试设计实验证明CaCO3以外的两种成分. 仅限选择的仪器和试剂:烧杯、试管、玻璃棒、滴管、药匙、漏斗、漏斗架;2 molL﹣1盐酸、2molL﹣1NaOH溶液、2%的KSCN溶液.
(1)将实验方案用以下流程示意图表示,试写出每步所用试剂的名称或化学式. 
试剂Ⅰ;试剂Ⅱ;试剂Ⅲ .
(2)如果猜测是成立的,试根据上述实验方案,叙述实验操作,预期现象和结论.
编号 | 实验操作 | 预期现象和结论 |
① | 取适量矿石研细,加 | 有大量无色气体生成,得棕黄 |
② | ||
③ | ||
④ |