题目内容
下列说法不正确的是
A.标准状况下,等体积的CH4和CO2所含的共用电子对数相等
B.与NaOH溶液、H2SO4溶液反应产生等量的H2,所需铝粉的质量相等
C.明矾溶液中K +和A13+的物质的量浓度相等
D.1molOH-和17gNH3所含的电子数相等
 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案下列离子方程式的书写及评价,均合理的是( )
选项 | 离子方程式 | 评价 |
A | 将少量的Fe3O4溶解在过量的稀HNO3中Fe3O4+8H+=Fe2++2Fe3++4H2O | 正确,Fe2+与Fe3+物质的量之比为1:2 |
B | Ba(HCO3)2溶液与足量的NaOH溶液反应 Ba2++HCO3-+OH-=BaCO3↓+H2O | 正确;酸式盐与碱反应生成正盐和水 |
C | 过量SO2通入到NaClO溶液中: SO2+H2O+ClO-=HClO+HSO3- | 正确;说明酸性:H2SO3强于HClO |
D | 1mol/L的NaAlO2溶液和2.5mol/L的HCl溶液等体积互相均匀混合: 2AlO2-+5H+=Al3++Al(OH)3↓+H2O | 正确;AlO2-与Al(OH)3消耗的H+的物质的量之比为2∶3 |
短周期元求X、Y、W在元素周期表中的相对位置如下图所示,其中Z为地壳中含量最高的金属元素。下列说法正确的是
|
|
|
|
|
| X |
Y |
| Z |
|
|
| W |
A.工业上电解YW饱和溶液冶炼金属Y
B.气态氢化物的稳定性:W>X
C.简单离子半径的大小顺序:r(Y+)>r(X-)
D.Y、W的最高价氧化物的水化物均能溶解金厲Z
在500℃时,将足量的A固体投入2.0L真空密闭容器中,
发生A(s) 2B(g)+C(g)反应,测得气体C随时间的浓度变化如下图所示
2B(g)+C(g)反应,测得气体C随时间的浓度变化如下图所示
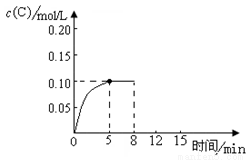
(1)已知该反应只有高温下能自发进行,则该反应的△H 0(填“>”、“<”或“=”)。
(2)在上述反应条件下,从反应开始到平衡,用B表示的化学反应速率为v(B)= mol·L-1·min-1,500℃时的平衡常数K= ;
(3)甲烷是一种常见的清洁能源:
①若800 ℃时,反应CH4(g)+H2O(g) CO(g)+3H2(g) ΔH=+206.1 kJ·mol-1的平衡常数(K)=1.0,某时刻测得该温度下密闭容器中各物质的物质的量浓度如下表:
CO(g)+3H2(g) ΔH=+206.1 kJ·mol-1的平衡常数(K)=1.0,某时刻测得该温度下密闭容器中各物质的物质的量浓度如下表:
CH4 | H | CO | H2 |
3.0 mol·L-1 | 8.5 mol·L-1 | 2.0 mol·L-1 | 2.0 mol·L-1 |
则此时正、逆反应速率的关系是 。(填标号)
A.v(正)<v(逆) B.v(正)=v(逆) C.v(正)>v(逆) D.无法判断



 2CeT3(有机层)+6H+(水层)
2CeT3(有机层)+6H+(水层)
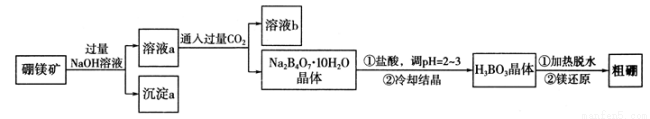
 2B4O7·10H2O与盐酸反应的化学方程式:_____________________。
2B4O7·10H2O与盐酸反应的化学方程式:_____________________。
 O2和N2,下列说法正确的是
O2和N2,下列说法正确的是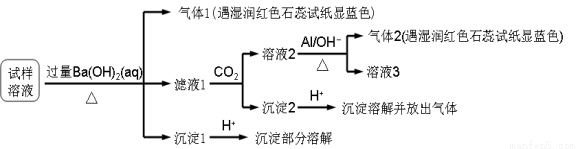
 2O
2O