��Ŀ����
����Ŀ���л���A������ʳƷ��ҵ����֪9.0g A������O2�г��ȼ�գ������ɵĻ����������ͨ��������Ũ����ͼ�ʯ�ң��ֱ�����5.4g��13.2g��������ʣ������ΪO2 ��
��1��A���ӵ�����ͼ��ͼ��ʾ����ͼ�п�֪����Է��������� �� ��A�ķ���ʽ���� 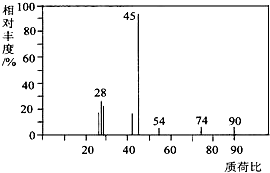
��2��A����NaHCO3��Һ������Ӧ��Aһ�����еĹ���������
��3��A���ӵĺ˴Ź���������4�����շ壬�����֮����1��1��1��3����A�Ľṹ��ʽ��
��4����д����������A��ͬ��ͬ���칹��Ľṹ��ʽ ��
���𰸡�
��1��90��C3H6O3
��2���Ȼ�
��3��CH3CH��OH��COOH
��4��HOCH2CH2COOH
���������⣺��1����ͼA���ӵ�����ͼ����֪A����Է�������Ϊ90��9gA�����ʵ���Ϊ ![]() =0.1mol��ȼ�����ɶ�����̼Ϊ
=0.1mol��ȼ�����ɶ�����̼Ϊ ![]() =0.3mol������ˮΪ
=0.3mol������ˮΪ ![]() =0.3mol�����л��������N��C��=
=0.3mol������������N��C��= ![]() =3��N��H��=
=3��N��H��= ![]() =6���������N��O��=
=6���������N��O��= ![]() =3�����л���A�ķ���ʽΪ��C3H6O3 ��
=3�����л���A�ķ���ʽΪ��C3H6O3 ��
�ʴ�Ϊ��90��C3H6O3����2��A����NaHCO3��Һ������Ӧ��Aһ�������Ȼ����ʴ�Ϊ���Ȼ�����3���л���A�ķ���ʽΪ��C3H6O3 �� �����Ȼ���A���ӵĺ˴Ź���������4�����շ壬˵������4��Hԭ�ӣ������֮����1��1��1��3����4��Hԭ����Ŀ��Ϊ1��1��1��4����A�Ľṹ��ʽΪ��CH3CH��OH��COOH��
�ʴ�Ϊ��CH3CH��OH��COOH����4����������A��ͬ��ͬ���칹��Ľṹ��ʽ��HOCH2CH2COOH��
�ʴ�Ϊ��HOCH2CH2COOH��
��1����ͼA���ӵ�����ͼ����֪A����Է�������Ϊ90�������л���A��������̼��ˮ�����ʵ���������ԭ���غ�ȷ��C��Hԭ����Ŀ�������Է�������ȷ����ԭ����Ŀ������ȷ���л������ʽ����2��A����NaHCO3��Һ������Ӧ��Aһ�������Ȼ�����3��A���ӵĺ˴Ź���������4�����շ壬˵������4��Hԭ�ӣ������֮����1��1��1��3����4��Hԭ����Ŀ��Ϊ1��1��1��4������л������ʽ�뺬�еĹ�����ȷ����ṹ��ʽ����4�����A�Ľṹ��ʽ��д��������ͬ��A���ܵ�ͬ���칹�壮

 ����ͬѧһ����ʦȫ�źþ�ϵ�д�
����ͬѧһ����ʦȫ�źþ�ϵ�д�