��Ŀ����
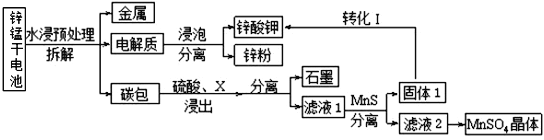
����Ŀ���ҹ��Ǹɵ�ص����������Ѵ����ij�����Ŷ�������������̶ԷϾɼ���п�̸ɵ�ص���Դ���л��գ�
��֪��
��Ksp(MnS)=2.5��10��13��Ksp(ZnS)=1.6��10��24
��Mn(OH)2��ʼ����ʱpHΪ8.3����ȫ������pHΪ9.8
�� 0.1 mol/L NaHCO3��Һ��pHԼΪ8��0.1 mol/L Na2CO3��Һ��pHԼΪ11��
(1)����п�̸ɵ������п��Ϊ��������������Ϊ����������������ҺΪ����ʡ�����ܷ�ӦΪ��2MnO2+Zn+2KOH= 2MnOOH+K2ZnO2����д����ص�������Ӧʽ________________________________��
(2)Ϊ�����̼���Ľ���Ч�ʣ����Բ�ȡ�Ĵ�ʩ��______________________________��(дһ������)
(3)����Һ1�м���MnS��Ŀ����__________________________________________��
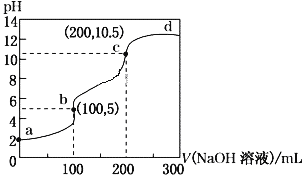
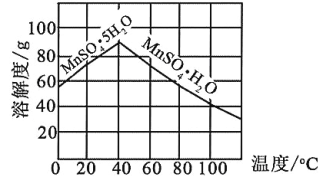
(4)��֪MnSO4���ܽ��������ͼ��ʾ������Һ2������MnSO4��H2O����IJ����������ᾧ��____________________��ϴ�ӡ����¸��
(5)Ϊ��ѡ���Լ�X������ͬ�����£��ֱ���3 g̼�������Ʊ�MnSO4��ʵ�飬�õ��������±�����д������Լ�X��̼���е���Ҫ�ɷַ�����Ӧ�Ļ�ѧ����ʽ________________��
ʵ���� | �Լ�X | MnSO4/g |
1 | � | 2.4 |
2 | ���� | 2.7 |
3 | FeS��ĩ | 3.0 |
4 | 30%�������� | 3.7 |
(6)��ҵ�Ͼ�����������Һ2�м���NaHCO3��Һ���Ʊ�MnCO3����ѡ��Na2CO3��Һ��ԭ����_______________________________________��
(7)�ÿ���С������EDTA(�Ҷ�����������ƣ������Ӽ�дΪY2��)������ϵζ����ⶨMnԪ���ڵ���е������ٷ�����
ʵ��������£�
�ٽ�һ�ڷϾɼ���п�̸ɵ�ز���ȥ��������̼���Լ����װ��
��ȷ��ȡ�����ĩ1.200 g��
�۾���ˮ�����Ȳ���õ���Һ1(<100 mL)��
�ܽ���Һ1ϡ����100.00 mL��
��ȡ20.00 mL��Һ��0.0500 molL��1EDTA����Һ�ζ�����һ�������£�ֻ������Ӧ��Mn2++Y2��=MnY��
���ظ��ζ�3�Σ�ƽ�����ı���Һ22.00 mL��
��MnԪ�ص������ٷ���Ϊ________��(����3λ��Ч����)
���𰸡�MnO2+H2O +e��= MnOOH+OH�� �ʵ�������(�����) ����Һ�е�Zn2+ת��ΪZnS��������ȥ ���ȹ��� H2O2+MnO2+H2SO4=MnSO4+2H2O+O2����H2O2+ 2MnOOH+2H2SO4=2MnSO4+4H2O+O2�� Na2CO3��Һ�ļ���ǿ�����ײ���Mn(OH)2�ij��� 25.2%
��������
п�̸ɵ��ˮ����ִ����õ�����Ϊп,����ʽ��ݹ��˷���õ�п�ۺ�п���,̼�����������������,����õ�ʯī����Һ1,����MnS����п����������п,���˵õ���Һ2Ϊ������,��пת��Ϊп�������MnSO4���ܽ�����߿���֪��, MnSO4��H2O���¶ȳ���40![]() ���ܽ�����¶ȵ����߶�����,����Һ2��Һ�����ᾧ�����ȹ��ˡ�ϴ�ӡ������¸���õ�MnSO4��H2O����;
���ܽ�����¶ȵ����߶�����,����Һ2��Һ�����ᾧ�����ȹ��ˡ�ϴ�ӡ������¸���õ�MnSO4��H2O����;
��1���ɵ�ص��ܷ�Ӧ֪���ŵ�ʱ�����������������õ��ӣ��ڼ����������������������̣������ķ�Ӧ����ʽΪMnO2+H2O +e��= MnOOH+OH�����𰸣�MnO2+H2O +e��= MnOOH+OH����
��2��Ϊ�����̼���Ľ���Ч�ʣ��ɽ�̼�����飬����Ӵ���������ʵ�������(�����) �ӿ���������ʡ��𰸣��ʵ�������(�����)��ɽ�̼��������
��3��������Ŀ����Ϣ����п���ܽ��ԶС�����̣������̵�Ŀ����ʹ��Һ�е�п����ת��Ϊ��п�������Ҳ��������������������ӡ��𰸣�����Һ�е�Zn2+ת��ΪZnS��������ȥ��
��4��MnSO4��H2O���������¶ȵ����ߣ��ܽ����С���ʴ���Һ2������MnSO4��H2O����IJ����������ᾧ�����ȹ�����ϴ�ӡ����¸���𰸣����ȹ��ˡ�
��5���ɱ�֪���Լ�XΪ30%��������ʱ��Ŀ�������������̼���ijɷֶ������̺����ᡢ��������ķ�Ӧ����ʽΪH2O2+MnO2+H2SO4=MnSO4+2H2O+O2����H2O2+ 2MnOOH+2H2SO4=2MnSO4+4H2O+O2�� ���𰸣�H2O2+MnO2+H2SO4=MnSO4+2H2O+O2����H2O2+ 2MnOOH+2H2SO4=2MnSO4+4H2O+O2����
��6����֪��Mn(OH)2��ʼ����ʱpHΪ8.3,��ȫ������pHΪ9.8��̼������Һ�ļ���ǿ��̼�����ƣ���̼���ƣ���ʹ������ת��Ϊ�������̳��������ٲ�Ʒ�IJ������𰸣�Na2CO3��Һ�ļ���ǿ�����ײ���Mn(OH)2�ij�����
��7������EDTA����Һ���ʵ���=0.0500mol/L![]() 0.0220L=0.0011mol,Mn2++Y2-= MnY ,����Ʒ��Mn2+�����ʵ���Ϊ0.0011mol
0.0220L=0.0011mol,Mn2++Y2-= MnY ,����Ʒ��Mn2+�����ʵ���Ϊ0.0011mol![]()
![]() =0.11molԪ���غ�õ�MnԪ�صİٷֺ�=
=0.11molԪ���غ�õ�MnԪ�صİٷֺ�=![]() 100
100![]() =25.2%��˴���: 25.2%��
=25.2%��˴���: 25.2%��

����Ŀ��ij�¶��£��ڼס��ҡ��������ĸ������ܱ�������Ͷ��H2��I2��������Ӧ��H2 (g) +I2 (g)![]() 2HI(g)����Ӧ��ϵ�и�����Ũ�ȵ��й��������¡�
2HI(g)����Ӧ��ϵ�и�����Ũ�ȵ��й��������¡�
���� | ��ʼŨ�� | ƽ��Ũ�� | |
c(H2)/mol��L-1 | c(I2)/mol��L-1 | c(HI)/mol��L-1 | |
�� | 0.01 | 0.01 | 0.004 |
�� | 0.01 | 0.02 | a |
�� | 0.02 | 0.01 | b |
�� | 0.02 | 0.02 | ���� |
�����ж���ȷ����
A. HI��ƽ��Ũ�ȣ�a=b>0.004
B. ƽ��ʱ��H2��ת���ʣ���>��
C. ƽ��ʱ������H2��ת���ʵ���20%
D. ���������£��÷�Ӧ��ƽ�ⳣ��K=4