题目内容
【题目】磷、铁及它们化合物在生产生活及科研中应用广泛。
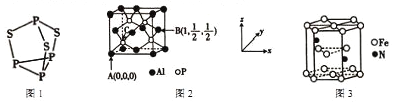
(1)P4S3可用于制造火柴,其分子结构如图1所示。
①P4S3分子中硫原子的杂化轨道类型为 ________________。
②每个P4S3分子中含孤电子对的数目为_________________。
(2)磷化铝熔点为2000℃,它与晶体硅互为等电子体,磷化铝晶胞结构如图2所示。
①磷化铝晶体中磷与铝微粒间的作用力为_______________。
②图中A点和B点的原子坐标参数如图所示, 则C点的原子坐标参数为_____________。
(3)Fe3+、Co3-与N3-、CN-等可形成络合离子。
①C、N、O的第一电离能最大的为____________,其原因是________________________________。
②K3[Fe(CN)6]可用于检验Fe2+, lmol[Fe(CN)6]3-离子中含有σ键的数目为__________________。
③[Co(N3)(NH3)5]SO4中Co的配位数为_____________。
(4)化合物FeF3熔点高于1000℃,而Fe(CO)5的熔点却低于0℃, FeF3熔点远高于Fe(CO)5的可能原因是__________________________________________________。
(5)某种磁性氮化铁晶体的结构如图 3所示,该化合物的化学式为_______________。
【答案】 sp3 10 极性共价键(或共价键) (1/4,1/4,1/4) N 氮原子2p轨道上的电子半充满,相对稳定,更不易失去电子 12NA 6 FeF3是离子晶体,Fe(CO)5是分子晶体,离子键的作用远比分子间作用力强,故FeF3的熔点Fe(CO)5。 Fe3N
【解析】(1)①分子中S原子形成2个共价键,孤对电子数为![]() (6-2×1)=2,则共有4个价层电子对,其杂化轨道类型为sp3;
(6-2×1)=2,则共有4个价层电子对,其杂化轨道类型为sp3;
②每个P4S3分子硫原子有2个孤对电子,P原子有孤对电子数为![]() (5-3×1)=1,则分子共含孤电子对的数目为10;
(5-3×1)=1,则分子共含孤电子对的数目为10;
(2)①磷化铝晶体中磷与铝之间形成极性共价键;
②图2中A点坐标参数为(0、0、0)、B点坐标参数为(1、![]() 、
、![]() ),说明晶胞边长为1,AC点距离为晶胞对角线的
),说明晶胞边长为1,AC点距离为晶胞对角线的![]() ,则C点的原子坐标参数为(
,则C点的原子坐标参数为(![]() 、
、![]() 、
、![]() );
);
(3)①C、N、O的第一电离能随核电荷数递增呈增大趋势,因N的2p轨道为半充满结构,更不易失去电子,第一电离相对较大,则C、N、O的第一电离最大的为N;
②[Fe(CN)6]3-中中心原子为Fe3+,CN-为配体,存在6个配位键,C与N之间为叁键,其中有一个键为σ键,lmol[Fe(CN)6]3-离子中含有σ键的数目为12NA;
③[Co(N3)(NH3)5]SO4中配体为N3-和NH3,SO42-为外界,则中心原子Co的配位数为6;
(4)FeF3是离子晶体,Fe(CO)5是分子晶体,离子键的作用远比分子间作用力强,故FeF3的熔点远高于Fe(CO)5。
(5)晶胞中Fe的原子个数为12×![]() +2×
+2×![]() +3=6,N原子个数为2,Fe与N原子个数比为3:1,则该化合物的化学式为Fe3N。
+3=6,N原子个数为2,Fe与N原子个数比为3:1,则该化合物的化学式为Fe3N。

 特高级教师点拨系列答案
特高级教师点拨系列答案【题目】某兴趣小组设计出如图所示装置来改进教材中“铜与硝酸反应”实验,以探究化学实验的绿色化。
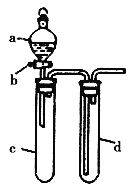
(1)实验前,关闭活塞b,试管d中加水至浸没长导管口,塞紧试管c和d的胶塞,加热c,其目的是_____________________。
(2)在d中加适量NaOH溶液,c中放一小块铜片,由分液漏斗a向c中加入2 mL浓硝酸,c中反应的化学方程式是______________________________________________。
(3)下表是制取硝酸铜的三种方案,能体现绿色化学理念的最佳方案是____________。
方案 | 反应物 |
甲 | Cu、浓HNO3 |
乙 | Cu、稀HNO3 |
丙 | Cu、O2、稀HNO3 |
(4)该小组还用上述装置进行实验证明酸性:HCl>H2CO3>H2SiO3,则分液漏斗a中加入的试剂是____________,c中加入的试剂是____________,d中加入的试剂是____________,实验现象为____________________________________________。有同学认为,该实验装置仍不能证明上述结论,改进的措施是_________________________________________。