题目内容
17.下列表示对应化学反应的离子方程式正确的是( )| A. | 向醋酸钠水溶液中通入少量CO2:2CH3COO-+CO2+H2O═2CH3COOH+CO32- | |
| B. | 向FeBr2溶液中通过量的Cl2:2Fe2++2Br-+2Cl2═2Fe3++4Cl-+Br2 | |
| C. | 向FeCl3溶液中加入Mg(OH)2:3Mg(OH)2+2Fe3+═2Fe(OH)3+3Mg2+ | |
| D. | 用浓盐酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性:2MnO${\;}_{4}^{-}$+6H++5H2O2═2Mn2++5O2↑+8H2O |
分析 A.碳酸的酸性比醋酸的弱;
B.亚铁离子、溴离子均全部被氧化;
C.发生沉淀转化;
D.盐酸能被高锰酸钾氧化.
解答 解:A.向醋酸钠水溶液中通入少量CO2,不发生离子反应,故A错误;
B.向FeBr2溶液中通过量的Cl2的离子反应为2Fe2++4Br-+3Cl2═2Fe3++6Cl-+2Br2,故B错误;
C.向FeCl3溶液中加入Mg(OH)2的离子反应为3Mg(OH)2+2Fe3+═2Fe(OH)3+3Mg2+,故C正确;
D.盐酸、过氧化氢均能与高锰酸钾发生氧化还原反应,则用浓盐酸酸化的KMnO4溶液与H2O2反应,不能证明H2O2具有还原性,故D错误;
故选C.
点评 本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应方程式书写的方法为解答的关键,侧重氧化还原反应、沉淀转化的离子反应考查,注意离子反应中保留化学式的物质及电子、电荷守恒,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
7.下列关于物质的量的叙述中,正确的是( )
| A. | 1 mol任何物质都含有6.02×1023个分子 | |
| B. | 12g 12C中含有约6.02×1023个碳分子 | |
| C. | 1 mol水中含有2 mol氢元素和1 mol氧元素 | |
| D. | 1 mol Ne中含有约6.02×1024个电子 |
8.下列实验操作不能达到实验目的是( )
| 选项 | 实验目的 | 实验操作 |
| A | 证明乙烯有还原性 | 将乙烯气体通入酸性KMnO4溶液中 |
| B | 比较H2O和乙醇中羟基氢的活泼性 | 分别加入少量Na |
| C | 检验溴乙烷中的溴原子 | 加入NaOH溶液,加热,然后加入AgNO3溶液 |
| D | 鉴别1-丙醇和2-丙醇 | 核磁共振氢谱 |
| A. | A | B. | B | C. | C | D. | D |
7.下列醇或卤代烃在合适条件下,也不能产生烯烃的是( )
| A. |  | B. | CH3Br | C. |  | D. |  |

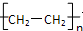
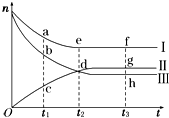 合成氨工业对国民经济和社会发展具有重要的意义.对于密闭容器中的反应:N2(g)+3H2(g)?2NH3(g),500K、30MPa下n(NH3)、n(H2)和n(N2)随时间变化的关系如图所示.
合成氨工业对国民经济和社会发展具有重要的意义.对于密闭容器中的反应:N2(g)+3H2(g)?2NH3(g),500K、30MPa下n(NH3)、n(H2)和n(N2)随时间变化的关系如图所示.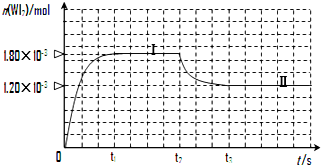 碘钨灯具有使用寿命长、节能环保等优点.一定温度下,在碘钨灯灯泡内封存的少量碘与沉积在灯泡壁上的钨可以发生如下的可逆反应:W(s)+I2(g)?WI2(g)
碘钨灯具有使用寿命长、节能环保等优点.一定温度下,在碘钨灯灯泡内封存的少量碘与沉积在灯泡壁上的钨可以发生如下的可逆反应:W(s)+I2(g)?WI2(g)