��Ŀ����
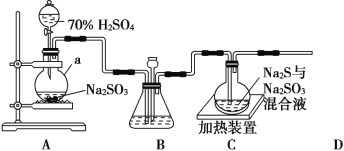
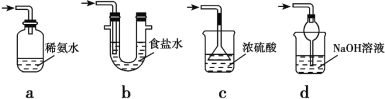
����Ŀ��a��b��c��d ��������֮���ת����ϵ��ͼ��ʾ(���ֲ�����ȥ)������˵����ȷ����

A. �� a Ϊ Cl2��b ����Ϊ NH3��ʵ���ҿ��ü��ȹ��� c �ķ�����ȡ NH3
B. �� a Ϊ Fe��b ����Ϊϡ HNO3����Ӧ�������ӷ���ʽΪ3Fe��8H+��2NO3-===3Fe2+��2NO2����4H2O
C. �� a Ϊ AlCl3 ��Һ��b ����Ϊ��ˮ����Ӧ�������ӷ���ʽΪAl3+��4NH3 ��H2O===AlO2-��4NH4+��2H2O
D. �� a Ϊ NaOH ��Һ��b ����Ϊ CO2������ Ca(OH)2 ��Һ���� c��d ��Һ�е�������
���𰸡�B
��������
A.��aΪCl2��b����ΪNH3������cΪ�Ȼ�泥����ڰ������Ȼ��ⷴӦ����ͨ�������Ȼ�淋ķ�����ȡNH3����A����
B.��aΪFe��b����ΪϡHNO3����Ӧ����������������Ӧ�����ӷ���ʽΪ��3Fe+8H++2NO3-�T3Fe2++2NO��+4H2O����B��ȷ��
C.��aΪAlCl3��Һ��b����Ϊ��ˮ���Ȼ����백ˮ��Ӧ��������������������ȷ�����ӷ���ʽΪ��Al3++3NH3H2O=Al��OH��3��+3NH4+����C����
D.��aΪNaOH��Һ��b����ΪCO2��cΪ̼�����ƣ�dΪ̼���ƣ�̼���ƺ�̼�����ƶ�������������Һ��Ӧ����̼��Ƴ���������Ca��OH��2��Һ��������D����
��ѡB��

 ��������ܸ�ϰϵ�д�
��������ܸ�ϰϵ�д�����Ŀ��2SO2(g) + O2(g) ![]() 2SO3(g)�ǹ�ҵ���������Ҫ��Ӧ֮һ��һ���¶��£��ڼס��ҡ��������ݻ���Ϊ2 L�ĺ����ܱ�������Ͷ��SO2(g)��O2(g)������ʼ���ʵ�����SO2��ƽ��ת�������±���ʾ�������ж��У���ȷ����
2SO3(g)�ǹ�ҵ���������Ҫ��Ӧ֮һ��һ���¶��£��ڼס��ҡ��������ݻ���Ϊ2 L�ĺ����ܱ�������Ͷ��SO2(g)��O2(g)������ʼ���ʵ�����SO2��ƽ��ת�������±���ʾ�������ж��У���ȷ����
�� | �� | �� | ||
��ʼ���ʵ��� | n(SO2) / mol | 0.4 | 0.8 | 0.8 |
n(O2) / mol | 0.24 | 0.24 | 0.48 | |
SO2��ƽ��ת���� / % | 80 | ��1 | ��2 | |
A. ���з�Ӧ��ƽ�ⳣ��С����
B. ƽ��ʱ������c(SO3)�Ǽ��е�2��
C. ���¶��£�ƽ�ⳣ��ֵΪ400
D. ƽ��ʱ������O2��ת���ʴ�������O2��ת����