题目内容
下列物质转化在给定条件下能实现的是
①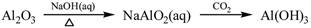
②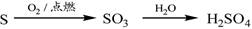
③
④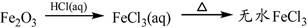
⑤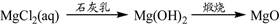
| A.①③⑤ | B.①④⑤ | C.②③④ | D.②④⑤ |
A
解析试题分析:Al2O3是两性氧化物,Al(OH)3是两性氢氧化物,则Al2O3 (s)+2NaOH(aq)=2NaAlO2(aq)+H2O(l),NaAlO2(aq)+2H2O(l)+CO2(g)=Al(OH)3↓+NaHCO3,所以①能;S是易燃物,但是其燃烧产物只有SO2,在催化剂条件下SO2才能转化SO3,故②不能;NH3+H2O+CO2=NH4HCO3,NH4HCO3+NaCl=NaHCO3↓+NH4Cl,2NaHCO3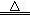 Na2CO3+CO2↑+H2O,故③能;Fe2O3是碱性氧化物,Fe2O3(s)+6HCl(aq)=2FeCl3(aq)+3H2O(l),FeCl3是强酸弱碱盐,加热能使其溶液中的FeCl3彻底水解,不仅逸出HCl气体,得到的Fe(OH)3受热易分解,最终不能得到无水FeCl3固体,而是得到Fe2O3固体,故④不能;溶解度:Ca(OH)2>Mg(OH)2,则MgCl2(aq)+ Ca(OH)2=Mg(OH)2+CaCl2(aq),Mg(OH)2是难溶性碱,受热易分解,煅烧可以得到熔沸点高的MgO固体和水蒸气,故⑤能;综上所述,①③⑤能实现指定物质间的转化,而②④则不能实现指定物质间的转化,故选A。
Na2CO3+CO2↑+H2O,故③能;Fe2O3是碱性氧化物,Fe2O3(s)+6HCl(aq)=2FeCl3(aq)+3H2O(l),FeCl3是强酸弱碱盐,加热能使其溶液中的FeCl3彻底水解,不仅逸出HCl气体,得到的Fe(OH)3受热易分解,最终不能得到无水FeCl3固体,而是得到Fe2O3固体,故④不能;溶解度:Ca(OH)2>Mg(OH)2,则MgCl2(aq)+ Ca(OH)2=Mg(OH)2+CaCl2(aq),Mg(OH)2是难溶性碱,受热易分解,煅烧可以得到熔沸点高的MgO固体和水蒸气,故⑤能;综上所述,①③⑤能实现指定物质间的转化,而②④则不能实现指定物质间的转化,故选A。
考点:考查元素化合物的性质,涉及铝钠铁镁等金属元素及其化合物、硫碳氮氯等非金属元素及其化合物的重要性质、盐类水解等知识。

 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案下表各选项中,不能利用置换反应通过Y得到W的一组化合物是
| 选项 化合物 | A | B | C | D |
| Y | CO2 | Fe2O3 | HgS | FeCl3 |
| W | MgO | Al2O3 | SO2 | CuCl2 |
甲、乙、丙、丁、戊的相互转化关系如图所示(反应条件略去,箭头表示一步转化)。下列各组物质中,不满足图示转化关系的是
| | 甲 | 乙 | 丙 | 戊 |
| ① | NH3 | O2 | NO | H2O |
| ② | Fe | H2O | H2 | Fe2O3 |
| ③ | Al2O3 | NaOH溶液 | Na AlO2溶液 | 过量CO2 |
| ④ | Na2O2 | CO2 | O2 | Na |
A.①③ B.②③ C.②④ D.①④
根据下列有关实验得出的结论一定正确的是
| 选项 | 方法 | 结论 |
| A | 同温时,等质量的锌粒分别与足量稀硫酸反应 | 产生氢气量:加过胆矾=没加胆矾 |
| B | 向Fe(NO3)2溶液中滴入用硫酸酸化的H2O2溶液,则溶液变黄 | 氧化性:H2O2>Fe3+ |
| C | 相同温度下,等质量的大理石与等体积、等浓度的盐酸反应 | 反应速率:粉状大理石>块状大理石 |
| D | 向2mL 0.1mol·L-1Na2S溶液中滴入几滴0.1mol·L-1ZnSO4溶液,有白色沉淀生成;再加入几滴0.1mol·L-1 CuSO4溶液,则又有黑色沉淀生成 | 溶度积(Ksp):ZnS>CuS |
下列类推正确的是
| A.CaCO3与稀硝酸反应生成CO2,CaSO3也能与稀硝酸反应生成SO2 |
| B.铜在氯气中剧烈燃烧生成二价铜,铜也能在硫蒸气中剧烈燃烧生成二价铜 |
| C.锌可以与溶液中的银离子发生置换反应,钠也能与溶液中的银离子发生置换反应 |
| D.钠与乙醇反应产生氢气,钾与乙醇也能反应产生氢气 |
下列陈述I、II正确且有因果关系的是
| 选项 | 陈述I | 陈述II |
| A | SO2有漂白性 | SO2可使酸性高锰酸钾溶液褪色 |
| B | 硫酸铜是强酸弱碱盐 | 蒸干CuSO4溶液可以得到Cu(OH)2固体 |
| C | SO2是酸性氧化物 | 将SO2通入BaCl2溶液可生成BaSO3沉淀 |
| D | 氢氧化铝显两性 | 向AlCl3溶液中滴加氨水,产生白色沉淀;再加入过量NaOH溶液,沉淀消失 |
下列说法正确的是
A.用氯酸钾固体和浓盐酸制氯气的反应方程式: |
| B.向含有大量Ca2+、Cl—、Al3+的溶液中通入适量SO2,有沉淀生成 |
| C.用少量酸性KMnO4溶液可以检测FeCl3浓溶液中是否含有Fe2+ |
| D.常温下Ksp[Cu(OH)2]=2.2×10-20,则常温下2.2mol/L CuCl2溶液的pH不大于4 |