题目内容
| | | | | | | | | | | | | | | | | | |
| | | | | | | | | | | | | | | | A | | |
| B | | | | | | | | | | | | | | | C | | |
| | | | | | | | | | | | | | | | | | |
| | | | | | | | | | | | | | | | | | |
| | | | | | | | | | | | | | | | | | |
| | | | | | | | | | | | | | | | | | |
(2)在我们常用的周期表中,氢元素的位置比较尴尬,它是第1列的唯一非金属元素。请写出H2O的电子式: ,氢还能与许多金属形成金属氢化物比如NaH,试分析其中氢元素的化合价为 ,这样看来若把氢元素放在 族也有一定道理。
(3)元素B与元素C形成的化合物中,化学键类型为 。
(4)A、B、C的原子半径由大到小的顺序为 (用元素符号回答)。
(1)氧; 二; VIA ;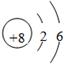 (2)
(2)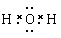 ; -1;ⅦA
; -1;ⅦA
(3)离子键 (4)Na > S > O
解析试题分析:(1)根据元素在周期表中的位置可知,A是氧元素,位于第二周期第ⅥA族,原子结构示意图是 。
。
(2)水是含有极性键的共价化合物,电子式是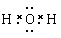 。金属钠只有+1价,所以在NaH中氢元素的化合价是-1价,据此可知氢元素放在第ⅦA族也是有道理的。
。金属钠只有+1价,所以在NaH中氢元素的化合价是-1价,据此可知氢元素放在第ⅦA族也是有道理的。
(3)元素B与元素C分别是是钠和S,形成的化合物是硫化钠,化学键类型为离子键。
(4)同主族自上而下原子半径逐渐增大,同周期自左向右原子半径逐渐减小,则A、B、C的原子半径由大到小的顺序为Na > S > O。
考点:考查元素周期表的结构、元素周期律的应用和判断以及常见化学用语的书写
点评:本题主要是元素“位、构、性”三者关系的综合考查,考查学生对表中各元素性质和相应原子结构的周期性递变规律的认识和掌握程度,有利于培养学生的逻辑推理能力和发散思维能力。

练习册系列答案
相关题目
请回答下列实验中的有关问题.
(1)实验室用浓硫酸与乙醇共热制取乙烯,以下是某同学设计的三套气体发生装置.
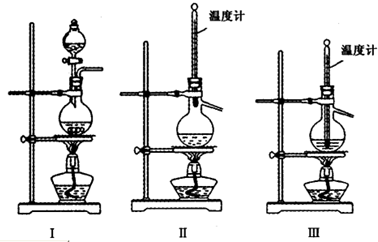
其中合理的是 (填序号),该装置中,反应容器的名称是 .
(2)利用如下实验装置制备氨气,并完成氨气的喷泉实验.
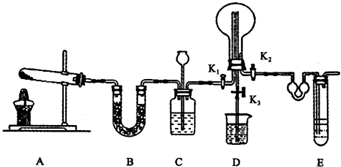
①请完成下表
②实验时,组装好装置后,下列步骤的正确顺序是 (填序号).
a.加入试剂 b.检查装置的气密性 c.关闭K1、K2,打开K3 d.关闭K3、打开K1、K2
e.给A装置试管进行加热 f.撤去酒精灯 g.用热毛巾敷盖在烧瓶上
③实验中,说明D部分烧瓶中氨气已经收集满的现象是 .
(1)实验室用浓硫酸与乙醇共热制取乙烯,以下是某同学设计的三套气体发生装置.

其中合理的是
(2)利用如下实验装置制备氨气,并完成氨气的喷泉实验.

①请完成下表
| 应加入试剂 | 所起作用 | A | B | C | 四氯化碳 | E | 检验氧气是否收集满 |
a.加入试剂 b.检查装置的气密性 c.关闭K1、K2,打开K3 d.关闭K3、打开K1、K2
e.给A装置试管进行加热 f.撤去酒精灯 g.用热毛巾敷盖在烧瓶上
③实验中,说明D部分烧瓶中氨气已经收集满的现象是
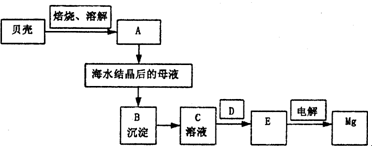
现有A、B、C、D四种钠的化合物,除一种为淡黄色外,其余均为白色粉末,已知四种物质可分别发生如下反应:
①A+C→B+H2O
②D+CO2→B+O2
③D+H2O→C+O2↑
④A→B+H2O+CO2
则A、B、C、D四种物质分别为( )
①A+C→B+H2O
②D+CO2→B+O2
③D+H2O→C+O2↑
④A→B+H2O+CO2
则A、B、C、D四种物质分别为( )
| A、NaHCO3、Na2CO3、NaOH、Na2O2 | B、Na2CO3、NaHCO3、NaOH、Na2O2 | C、NaHCO3、NaOH、Na2CO3、Na2O2 | D、NaOH、Na2CO3、NaHCO3、Na2O2 |
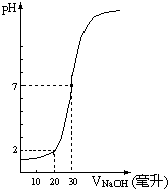 下图为10mL一定物质的量浓度的盐酸X,用一定物质的量浓度的NaOH溶液Y滴定的图示,据图推出NaOH溶液和盐酸的物质的量的浓度是( )
下图为10mL一定物质的量浓度的盐酸X,用一定物质的量浓度的NaOH溶液Y滴定的图示,据图推出NaOH溶液和盐酸的物质的量的浓度是( )