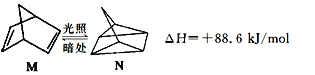
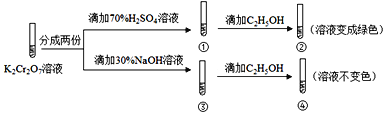
��Ŀ����
����Ŀ����֪���Ϊ2L�ĺ����ܱ������з�����Ӧ��2SO2��g�� + O2��g��![]() 2SO3��g��������ݻ�ѧ��Ӧ���й�ԭ��ͬ����������
2SO3��g��������ݻ�ѧ��Ӧ���й�ԭ��ͬ����������
��1��һ�������£�����2mol SO2��g����2mol O2��g����20s���SO2������ٷֺ���Ϊ12.5%������SO2��ʾ�÷�Ӧ����20s�ڵķ�Ӧ����Ϊ_____________________��
��2���������������Ϊ�жϣ�1���п��淴Ӧ�ﵽƽ��״̬���ݵ��ǣ�����ţ�___________��
�����������ܶȲ��� ����������ƽ����Է�����������
�� v����SO2��=2v����O2�� ���������Ũ�ȶ����ٷ����仯
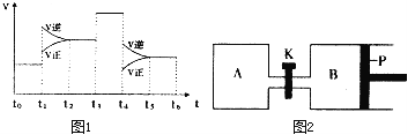
��3��ͼ1��ʾ�÷�Ӧ�����ʣ�v����ʱ�䣨t���ı仯�Ĺ�ϵ�������в�ͬʱ����У�SO3 �İٷֺ�����ߵ��ǣ� ��
A��t2��t3 B��t0��t1 C��t5��t6 D��t3��t4
��ͼ����������Ϊt3ʱ�ı���������������__________��
��4��ͼ2��P�ǿ�����ƽ�л����Ļ���������ͬ�¶�ʱ����A�����г���4mol SO3��g�����ر�K����B�����г���2mol SO3��g�����������ֱ�����Ӧ����֪��ʼʱ����A��B�������ΪaL���Իش�
����Ӧ�ﵽƽ��ʱ����B������Ϊ1.2a L������B��SO3ת����Ϊ___________��
������K��һ��ʱ������´ﵽƽ�⣬����B�����Ϊ___________L����ͨ��������������Բ��ƣ��Ҳ������¶ȵ�Ӱ�죩��
���𰸡���1��0.04mol/(L��s) ��2���ڢ�
��3��B �������� ��4��40% 2.6a
��������
�����������1���跴Ӧ�Ķ�������Ϊx����
2SO2��g�� + O2��g��![]() 2SO3��g��
2SO3��g��
��ʼ��mol���� 2 2 0
��Ӧ��mol���� 2x x 2x
ƽ�⣨mol���� 2-2x 2-x 2x
20s���SO2������ٷֺ���Ϊ12.5%����ͬ�����£��������������������ʵ�������������2-2x��/ [2-2x + (2-x) + 2x]��100%=12.5%�����x=0.8����Ӧ���ĵĶ�����������ʵ���Ϊ��2��0.8mol=1.6mol����SO2��ʾ�÷�Ӧ����20s�ڵķ�Ӧ����Ϊ��v��SO2��=(1.6mol/2L)/20s=0.04mol/��L/s����
��2�� ����Ӧǰ������������������ݻ������䣬����������ܶ�ʼ�ղ��䣬����˵����Ӧ�ﵽƽ��״̬���������������ƽ����Է��������ǻ�����������ͻ�������ܵ����ʵ����ı�ֵ���������䣬�����ʵ����DZ仯�ģ������������ƽ����Է��������������˵����Ӧ�ﵽƽ��״̬����ȷ���� v����SO2��=2v����O2������ʾ����Ӧ�������ʣ�����˵����Ӧ�ﵽƽ��״̬���������������Ũ�ȶ����ٷ����仯˵����Ӧ�ﵽƽ��״̬����ȷ����ѡ�ڢ���
��3������ͼ���֪��Ӧһֱ���淴Ӧ���������t3��t4ƽ�ⲻ�ƶ���˵���ı������Ӧ����ʹ���˴�����������SO3 �İٷֺ�����ߵ���t0��t1����ѡB��
��4������Ӧ�ﵽƽ��ʱ����B�����Ϊ1.2a L��BΪ��ѹ�����£��������ݻ�����������ʵ�������
�ȣ�˵���ﵽƽ��ʱ��������ʵ���Ϊ��Ӧǰ��1.2������ƽ��ʱ�����������ʵ���Ϊ2.4mol���跴Ӧ����������Ϊx����
2SO3��g��![]() 2SO2��g�� + O2��g��
2SO2��g�� + O2��g��
��ʼ��mol����2 0 0
��Ӧ��mol����x x 1/2x
ƽ�⣨mol����2-x x 1/2x
��2-x + x + 1/2x=2.4mol,x=0.8mol
���������ת����Ϊ��0.8mol/2mol��100%=40%��
������K��һ��ʱ������´ﵽƽ�⣬�ں��º�ѹ�����£�����B�н���6mol��������ﵽ��ƽ��Ϊ��Чƽ�⣬���Դﵽƽ��ʱ�����������ݻ�Ϊ��(6mol/2mol)��1.2aL=3.6aL����������B�����Ϊ��3.6aL-aL=2.6aL��