题目内容
【题目】己知:FeS2中S为-1价,Cu2S中S为-2价。对于反应l4CuSO4+5FeS2+12H2O =7Cu2S+5FeSO4+12H2SO4,下列说法正确的是( )
A.只有硫酸铜作氧化剂
B.SO42-既不是氧化产物又不是还原产物
C.被氧化的硫与被还原的硫的质量比为3:7
D.1 mol硫酸铜可以氧化5/7 mol的硫原子
【答案】C
【解析】
试题分析:A.该反应中Cu元素化合价由+2价变为+1价、S元素化合价由-1价变为+6价、-2价,根据元素化合价知,部分FeS2和硫酸铜作氧化剂,故A错误;B.因FeS2中部分S元素的化合价由-1升高到+6价,生成物中部分SO42-为氧化产物,故B错误;C.由反应可知,10个S原子中,有3个S原子失去电子,7个S原子得到电子,即被氧化的硫与被还原的硫的质量比为3:7,故C正确;D.1mol硫酸铜转移1mol电子,可以氧化硫原子的物质的量为![]() =
=![]() mol,故D错误;故选C。
mol,故D错误;故选C。

 快乐5加2金卷系列答案
快乐5加2金卷系列答案【题目】甲醇既可用于基本有机原料,又可作为燃料用于替代矿物燃料。
(1)以下是工业上合成甲醇的两个反应:
反应I: CO(g)+2H2(g)![]() CH3OH(g) ΔH1
CH3OH(g) ΔH1
反应II:CO2(g)+3H2(g)![]() CH3OH(g)+ H2O(g) ΔH2
CH3OH(g)+ H2O(g) ΔH2
① 上述反应符合“原子经济”原则的是 (填“I”或“II”)。
② 下表所列数据是反应I在不同温度下的化学平衡常数(K)。
温度 | 250℃ | 300℃ | 350℃ |
K | 2.041 | 0.270 | 0.012 |
由表中数据判断反应I为______________热反应(填“吸”或“放”)。
③ 某温度下,将2 mol CO和6 mol H2充入2L的密闭容器中,充分反应,达到平衡后,测得c(CO)= 0.2 mol/L,则CO的转化率为 ,此时的温度为 (从表中选择)。
(2) 已知在常温常压下:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g) ΔH1 kJ/mol
②2CO(g)+O2(g)=2CO2(g) ΔH2 kJ/mol
③H2O(g)=H2O(l) ΔH3 kJ/mol
则反应 CH3OH(l)+ O2(g)= CO(g)+ 2H2O(l) ΔH= kJ/mol
(3)现以甲醇燃料电池,采用电解法来处理酸性含铬废水(主要含有Cr2O72)时,实验室利用下图装置模拟该法:
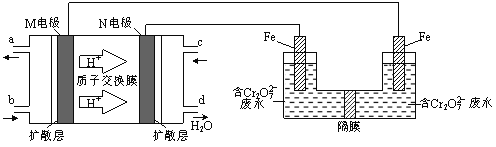
① N电极的电极反应式为 。
② 请完成电解池中Cr2O72转化为Cr3+的离子反应方程式:
Cr2O7 2+ Fe2+ + [ ] ═ Cr3++ Fe3++ [ ]
(4) 处理废水时,最后Cr3+以Cr(OH)3形式除去,当c(Cr3+)=1×105 molL﹣1 时,Cr3+沉淀完全,此时溶液的pH= 。 (已知, Ksp[Cr(OH)3]=6.4×1031,lg2=0.3)