题目内容
乙醇在能源、生产及日常生活等许多方面都有十分广泛的应用。请计算:
(1)将足量乙醇与9.2 g金属钠充分反应,则标准状况下生成气体的体积是 L
(2)若一定量的乙醇和O2在密闭容器中燃烧后的产物为CO2、CO和H2O(g)。产物依次经过浓硫酸和碱石灰使其被充分吸收,浓硫酸增重10.8 g,碱石灰增重13.2 g。则氧气的物质的量是 mol,燃烧产物的平均摩尔质量是 g/mol。
(1)4.48L ;(2)26.8g/mol
解析试题分析:(1)由题意:
2Na ~ H2↑
46g 22.4L
9.2g V(H2)
V(H2)=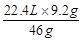 =4.48L .........................................................(2分)
=4.48L .........................................................(2分)
(2)根据氢原子守恒,可得:
C2H5OH ~ 3H2O
1mol 54g
n(C2H5OH) 10.8g
n(C2H5OH)=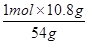 =0.2mol
=0.2mol
考点:考查有机物计算的相关知识点。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列有关物质的性质或应用的说法正确的是
| A.石油裂化的主要产品是甲烷、乙烯和苯 |
| B.除去乙醇中的少量水需加入氢氧化钙,再迸行蒸馏并灼烧 |
| C.盐析可提纯蛋白质并能保持蛋白质的生理活性 |
| D.木糖醇(C5H12O5)是一种甜味剂,与葡萄糠互为同系物 |
下列化学式不只表示一种物质的是( )
| A.C3H8 | B.C4H10 | C.CHCl3 | D.CH2Cl2 |
某有机物的结构简式如图所示,关于该物质的叙述错误的是( )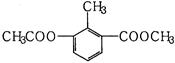
| A.一个分子中含有12个H原子 |
| B.苯环上的一氯代物有2种 |
| C.能使酸性KMnO4溶液褪色 |
| D.1mol该物质分别与足量H2、NaOH溶液反应,消耗其物质的量均为3mol |
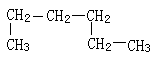
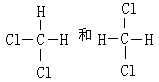 ③CH3—CH3和CH3—CH2—CH3
③CH3—CH3和CH3—CH2—CH3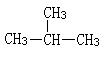
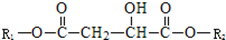
 。
。