题目内容
【题目】氮是生命的基础,由于存在着氮的循环,生命世界才能像我们所见到的那样生机勃勃,充满活力.如图是自然界中氮的循环图,请分析此图并回答有关问题.
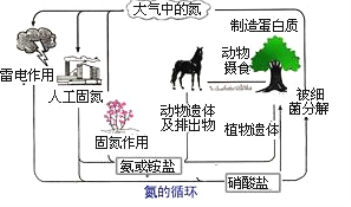
(1)大气中的氮以_____(填化学式)形式存在。图中共表示了_______种固氮的途径。
(2)由图可知,动植物体内的氮主要存在于蛋白质中,当动植物尸体发生腐败时,往往会产生一种含氮的气体,其电子式为___________。土壤中的硝酸盐会被细菌分解。有一种脱氧硫杆菌能够利用土壤中的硫化物来分解硝酸盐,其主要化学原理如下:K2S+KNO3+H2O![]() N2+K2SO4+KOH
N2+K2SO4+KOH
(3)上述反应中涉及1~18号元素的原子半径从大到小的顺序是_________________。属于共价化合物的反应物(或生成物)的结构式是_____________。
(4)配平上述反应方程式,并标出电子转移的方向和数目_____________。上述反应的氧化剂是_________________,被氧化的元素是____________________。
(5)上述过程的发生改变了土壤的成分,从而对农业生产产生一定的不利影响,请选择任一角度进行简要说明:_______________________。
(6)工业合成氨的简易流程如下图,通过循环Ⅰ可利用的气态物质是_____________

a.催化剂 b.只有N2 c.只有H2 d.N2和H2
【答案】 N2 3 ![]() S>N>O>H H—O—H 各物质系数5 8 4 4 5 8 转移电子数目40e KNO3
S>N>O>H H—O—H 各物质系数5 8 4 4 5 8 转移电子数目40e KNO3 ![]() 土壤中氮元素流失,肥力下降(合理即可) d
土壤中氮元素流失,肥力下降(合理即可) d
【解析】(1)大气中的氮以N2形式存在。图中共表示了3种固氮的途径,分别是闪电作用使N2被氧气氧化为NO,人工固氮及细菌的作用固氮;
(2)当动植物尸体发生腐败时,往往会产生一种含氮的气体NH3,其电子式为![]() ;
;
(3)上述反应中涉及1~18号元素有H、N、O、S,其中H原子半径最小,S为第三周期原子半径最大,N、O同周期,核电荷数大原子半径小,则四种元素的原子半径从大到小的顺序是S>N>O>H;反应物中的水为共价化合物,其结构式是H—O—H;
(4)在K2S + KNO3 + H2O![]() N2 + K2SO4 + KOH中S元素化合价从-2价升高为+6价,升8价,而N元素从+5价降为0价,每生成一个N2,降低10价,根据电子守恒可知,升高与降低化合价总数相等,则8和10的最小公倍数为40,即K2S前系数为5,而KNO3前系数为8,再结合原子守恒可得此反应方程式为5K2S + 8KNO3 + 4H2O
N2 + K2SO4 + KOH中S元素化合价从-2价升高为+6价,升8价,而N元素从+5价降为0价,每生成一个N2,降低10价,根据电子守恒可知,升高与降低化合价总数相等,则8和10的最小公倍数为40,即K2S前系数为5,而KNO3前系数为8,再结合原子守恒可得此反应方程式为5K2S + 8KNO3 + 4H2O![]() 4N2 + 5K2SO4 + 8KOH;此反应转移电子数为40,用单线桥分析转移电子数目及方向为
4N2 + 5K2SO4 + 8KOH;此反应转移电子数为40,用单线桥分析转移电子数目及方向为![]() ;此反应中N元素化合价降低,则KNO3是氧化剂,S元素化合价升高,被氧化;
;此反应中N元素化合价降低,则KNO3是氧化剂,S元素化合价升高,被氧化;
(5)上述过程的中KNO3被还原为N2,土壤中氮元素流失,肥力下降,另外产物为KOH,使土壤碱性化,不易作物生成;
(6)N2、H2在高温高压的条件下反应生成NH3,由图可知:流程中可循环利用的物质,故答案为d。