题目内容
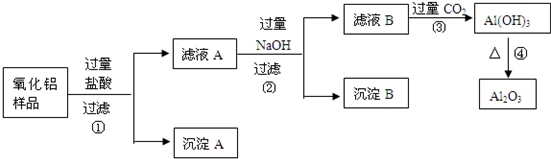
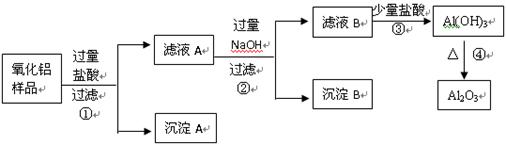
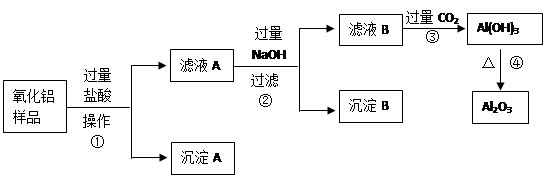
某氧化铝样品中含有氧化铁和二氧化硅杂质,现欲制取纯净的氧化铝,某同学设计如下的实验方案.
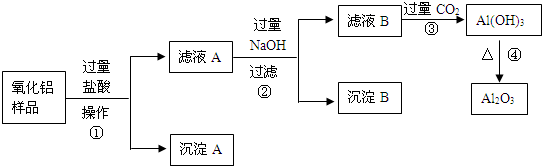
回答下列问题:
(1)操作①的名称 ;
(2)沉淀A的化学式是 ,滤液B中的阴离子除了Cl-、OH-外还有 ;
(3)步骤④的化学方程式为 ;
(4)在操作②中要用到的玻璃仪器除了烧杯、玻璃棒,还有 .

回答下列问题:
(1)操作①的名称
(2)沉淀A的化学式是
(3)步骤④的化学方程式为
(4)在操作②中要用到的玻璃仪器除了烧杯、玻璃棒,还有
分析:(1)不溶于水的固体和液体,可用过滤的方法分离;
(2)氧化铝样品中含有氧化铁和二氧化硅,氧化铁和氧化铝能与盐酸反应,而二氧化硅不与盐酸反应,滤液A中为氯化铝、氯化铁、盐酸;滤液B为偏铝酸钠和氢氧化钠和氯化钠的混合物;
(3)步骤④是氢氧化铝的分解,分解生成水和氧化铝,据此书写化学方程式;
(4)根据过滤操作用到的仪器来分析解答.
(2)氧化铝样品中含有氧化铁和二氧化硅,氧化铁和氧化铝能与盐酸反应,而二氧化硅不与盐酸反应,滤液A中为氯化铝、氯化铁、盐酸;滤液B为偏铝酸钠和氢氧化钠和氯化钠的混合物;
(3)步骤④是氢氧化铝的分解,分解生成水和氧化铝,据此书写化学方程式;
(4)根据过滤操作用到的仪器来分析解答.
解答:解:(1)氧化铝样品中含有氧化铁和二氧化硅杂质,加入过量盐酸,氧化铝与过量盐酸反应生成氯化铝,氧化铁和盐酸反应生成氯化铁,二氧化硅不与盐酸反应,沉淀A为SiO2,通过过滤进行固液分离,
故答案为:过滤;
(2)氧化铝样品中含有氧化铁和二氧化硅杂质,加入过量盐酸,氧化铝与过量盐酸反应生成氯化铝,氧化铁和盐酸反应生成氯化铁,二氧化硅不与盐酸反应,沉淀A为SiO2,滤液A中为氯化铝、氯化铁、盐酸,则滤液A中加入过量NaOH,氯化铝与碱反应生成偏铝酸钠和氯化钠,氯化铁与碱反应生成氢氧化铁沉淀和氯化钠,盐酸与碱反应生成氯化钠,则滤液B中有NaAlO2、NaCl、NaOH,所以滤液B中的阴离子除了Cl-、OH-外还有AlO2-,
故答案为:SiO2;AlO2-;
(3)氢氧化铝分解生成水和氧化铝,反应的化学方程式为:2Al(OH)3
3H2O↑+Al2O3,
故答案为:2Al(OH)3
3H2O↑+Al2O3;
(4)操作②为过滤操作,需要用到漏斗、玻璃棒、烧杯来完成过滤操作,故答案为:普通漏斗.
故答案为:过滤;
(2)氧化铝样品中含有氧化铁和二氧化硅杂质,加入过量盐酸,氧化铝与过量盐酸反应生成氯化铝,氧化铁和盐酸反应生成氯化铁,二氧化硅不与盐酸反应,沉淀A为SiO2,滤液A中为氯化铝、氯化铁、盐酸,则滤液A中加入过量NaOH,氯化铝与碱反应生成偏铝酸钠和氯化钠,氯化铁与碱反应生成氢氧化铁沉淀和氯化钠,盐酸与碱反应生成氯化钠,则滤液B中有NaAlO2、NaCl、NaOH,所以滤液B中的阴离子除了Cl-、OH-外还有AlO2-,
故答案为:SiO2;AlO2-;
(3)氢氧化铝分解生成水和氧化铝,反应的化学方程式为:2Al(OH)3
| ||
故答案为:2Al(OH)3
| ||
(4)操作②为过滤操作,需要用到漏斗、玻璃棒、烧杯来完成过滤操作,故答案为:普通漏斗.
点评:本题主要考查铁、铝、硅的化合物的性质,明确物质的性质及转化中发生的化学反应是解答本题的关键,题目难度中等.

练习册系列答案
 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案
相关题目