题目内容
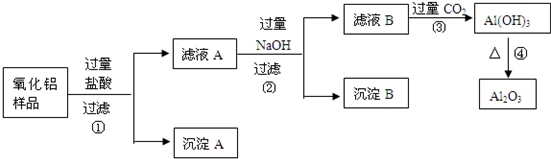
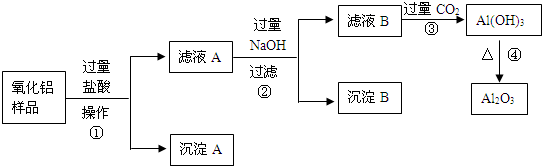
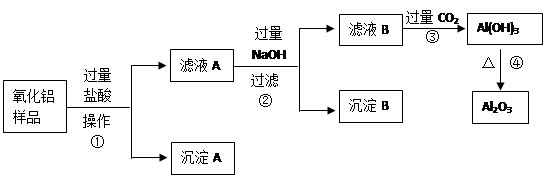
某氧化铝样品中含有氧化铁和二氧化硅杂质,(二氧化硅不溶于盐酸)现欲制取纯净的氧化铝,某同学设计如下的实验方案。回答下列问题:
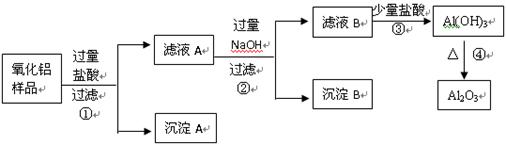
(1)沉淀A的化学式是________________,沉淀B的化学式是________________,滤液A中含有的阳离子为 和 ,滤液B中的含铝元素的化合物化学式是_________ ____;
(2)步骤②中,加过量的氢氧化钠发生的两个反应用化学方程式表示为:
,
。
(3)步骤③的离子方程式为 。
若所加的盐酸为过量,又能发生的反应的化学方程式为:
。
(4)在操作②中要用到的玻璃仪器有 、___________、__________。
(5)步骤④的反应化学方程式为_____________________________________。
(1)SiO2 Fe(OH)3 Fe3+ Al3+ Na[Al(OH)4]
(2)Fe3++3OH-= Fe(OH)3↓ Al3++4OH-=[Al(OH)4]-
(3)[Al(OH)4]-+H+ = Al(OH)3↓+ H2O Al(OH)3+3HCl = AlCl3+3H2O
(4)烧杯 玻璃棒 漏斗
|
(5)2Al(OH)3=== Al2O3+ 3H2O
解析: