ΧβΡΩΡΎ»ί
ΓΨΧβΡΩΓΩœρ“ΜΕ®ΝΩΒΡNaOH»ή“Κ÷–÷πΒΈΦ”»κAlCl3»ή“ΚΘ§…ζ≥…≥ΝΒμAlΘ®OHΘ©3ΒΡΝΩΥφAlCl3Φ”»κΝΩΒΡ±δΜ·ΙΊœΒ»γΆΦΥυ ΨΘ°‘ρœ¬Ν–άκΉ”Ήι‘ΎΕ‘”ΠΒΡ»ή“Κ÷–“ΜΕ®Ρή¥σΝΩΙ≤¥φΒΡ «Θ® Θ©
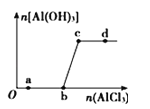
AΘ°aΒψΕ‘”ΠΒΡ»ή“Κ÷–ΘΚNa+ΓΔFe3+ΓΔSO42©¹ΓΔHCO3©¹
BΘ°bΒψΕ‘”ΠΒΡ»ή“Κ÷–ΘΚNa+ΓΔS2©¹ΓΔSO42©¹ΓΔCl©¹
CΘ°cΒψΕ‘”ΠΒΡ»ή“Κ÷–ΘΚAg+ΓΔCa2+ΓΔNO3©¹ΓΔNa+
DΘ°dΒψΕ‘”ΠΒΡ»ή“Κ÷–ΘΚK+ΓΔNH4+ΓΔI©¹ΓΔHCO3©¹
ΓΨ¥πΑΗΓΩB
ΓΨΫβΈωΓΩ
‘ΧβΖ÷ΈωΘΚaΒψ»ή÷ ΈΣNaOHΚΆNaAlO2Θ§Fe3ΘΪΓΔHCO3Θ≠ΚΆOHΘ≠≤ΜΡή¥σΝΩΙ≤¥φΘ§«“Fe3ΘΪΚΆHCO3Θ≠ΖΔ…ζΥΪΥ°ΫβΖ¥”ΠΘ§≤ΜΡή¥σΝΩΙ≤¥φΘ§Ι ¥μΈσΘΜBΓΔbΒψ»ή÷ «NaAlO2Θ§ΡήΙΜ¥σΝΩΙ≤¥φΘ§Ι ’ΐ»ΖΘΜCΓΔcΒψ»ή÷ ÷Μ”–NaClΘ§AgΘΪΚΆClΘ≠…ζ≥…AgCl≥ΝΒμΘ§≤ΜΡή¥σΝΩΙ≤¥φΘ§Ι ¥μΈσΘΜDΓΔdΒψAl3ΘΪΚΆHCO3Θ≠ΖΔ…ζΥΪΥ°ΫβΖ¥”ΠΘ§≤ΜΡή¥σΝΩΙ≤¥φΘ§Ι ¥μΈσΓΘ

ΓΨΧβΡΩΓΩΡ≥–Υ»Λ–ΓΉιΆ§―ß”ϊ―–ΨΩSO2ΒΡœύΙΊ–‘÷ ΓΘ
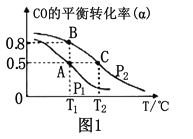
Θ®1Θ©±»Ϋœœ¬±μ÷–ΒΡΝΫΉιΈο÷ ΙΊœΒΘ§ΒΎ2Ήι÷–Έο÷ XΒΡΜ·―ß Ϋ « ΓΘ
ΒΎ1Ήι | ΒΎ2Ήι |
CΓΔCOΓΔCO2ΓΔH2CO3ΓΔNa2CO3ΓΔΓΔNaHCO3ΓΔ | S ΓΔSO2ΓΔSO3ΓΔXΓΔNa2SO4ΓΔNaHSO4 |
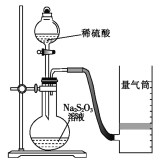
Θ®2Θ©άϊ”Οœ¬ΆΦΉΑ÷Οά¥Φλ―ιSO2ΒΡ–‘÷
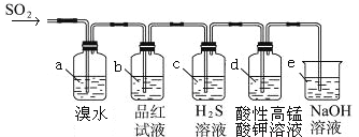
ΔΌΉΑ÷Οa÷–ΒΡœ÷œσ «ΘΚ ΘΜ Θ®ΧνΓΑΡήΓ±ΜρΓΑ≤ΜΡήΓ±Θ©ΥΒΟς SO2 ”–Τ·ΑΉ–‘
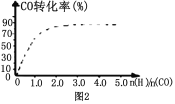
ΔΎ»τΉΑ÷Οe÷–”–40 mL 2Θ°5 molLΘ≠1 NaOH»ή“ΚΘ§Ζ¥”ΠΚσ‘ω÷Ί4Θ°8 gΘ§‘ρΉΑ÷ΟIV÷–ΖΔ…ζΖ¥”ΠΒΡΉήΜ·―ßΖΫ≥Χ Ϋ « ΓΘ
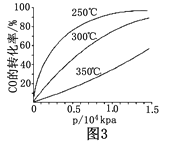
Θ®3Θ©ΗΟ–ΓΉιΒΡΦΉΓΔ““ΝΫΈΜΆ§―ßάϊ”Οœ¬ΆΦΉΑ÷ΟΦΧ–χΧΫΨΩSO2ΦΑ¬»ΤχΤ·ΑΉ–‘ΘΚ
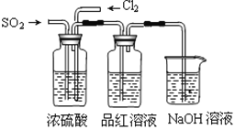
Ά®Τχ“ΜΕΈ ±ΦδΚσΘ§ΦΉΆ§―ß Β―ιΙΐ≥Χ÷–ΤΖΚλ»ή“ΚΦΗΚθ≤ΜΆ …ΪΘ§Εχ““Ά§―ßΒΡ Β―ιœ÷œσ «ΤΖΚλ»ή“ΚΥφ ±ΦδΒΡΆΤ“Τ±δΒΟ‘Ϋά¥‘Ϋ«≥ΓΘ ‘ΗυΨίΗΟ Β―ιΉΑ÷ΟΚΆΝΫΟϊΆ§―ßΒΡ Β―ιΫαΙϊΜΊ¥πΈ ΧβΓΘ
ΔΌ ‘Ζ÷ΈωΦΉΆ§―ß Β―ιΙΐ≥Χ÷–Θ§”ΟάκΉ”ΖΫ≥Χ Ϋ±μ ΨΤΖΚλ»ή“Κ≤ΜΆ …ΪΒΡ‘≠“ρ «ΘΚ ΓΘ
ΔΎΡψ»œΈΣ““Ά§―ß «‘θ―υΉωΒΫ»ΟΤΖΚλ»ή“Κ±δΒΟ‘Ϋά¥‘Ϋ«≥ΒΡΘΩ
ΓΘ