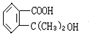题目内容
某有机物A的相对分子质量为62。为进一步测定A的化学式,现取6.2 gA完全燃烧,得到二氧化碳和水蒸气。将产物先后通过足量的浓硫酸和碱石灰,两者分别增重5.4 g和8.8 g (假设每步反应完全)。
(1)该有机物的实验式是 :分子式是 。
(2)红外光谱显示有“C—C”键和“O一H”键的振动吸收,若核磁共振氢谱有2个吸收峰,峰面积之比为1:2,推断该有机物的结构简式是 。
(3)该有机物与金属钠反应的化学方程式是 。
(1)CH3O C2H6O2 (2)HOCH2CH2OH
(3)HOCH2CH2OH+2Na NaOCH2CH2ONa+H2↑
NaOCH2CH2ONa+H2↑
【解析】
试题分析:(1)6.2gA的物质的量是0.1mol
生成的水是5.4g,物质的量是5.4g÷18g/mol=0.3mol,其中氢原子的物质的量是0.6mol
生成的CO2是8.8g,物质的量是8.8g÷44g/mol=0.2mol,其中碳原子的物质的量是0.2mol
所以根据原子守恒可知,A分子中含有的碳氢原子个数分别是2个和6个
则氧原子的个数是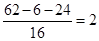 个
个
所以A的化学式是C2H6O2
(2)根据红外光谱和核磁共振氢谱可知,该有机物是乙二醇,结构简式是HOCH2CH2OH。
(3)醇能和金属钠反应生成氢气,则该反应的化学方程式是HOCH2CH2OH+2Na NaOCH2CH2ONa+H2↑
NaOCH2CH2ONa+H2↑
考点:考查有机物最简式、化学式、结构简式的有关判断和计算
点评:该题是高考中的常见考点和题型,属于中等难度试题的考查,试题综合性强,侧重对学生能力的培养和解题方法的指导与训练,旨在考查学生灵活运用基础知识解决实际问题的能力,有利于培养学生的逻辑推理能力和发散思维能力,提升学生的学科素养。该题的关键是利用好守恒法,即质量守恒定律、原子守恒等。