题目内容
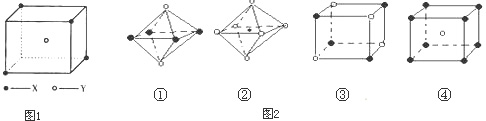
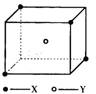
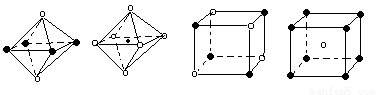
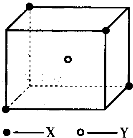 某离子晶体晶胞结构如图所示,x位于立方体的顶点,Y位于立方体中心.试分析:
某离子晶体晶胞结构如图所示,x位于立方体的顶点,Y位于立方体中心.试分析:该晶体的化学式为
XY2或Y2X.
XY2或Y2X.
.分析:晶胞中位于立方体顶点的离子被8个晶胞共有,位于立方体中心的离子被一个晶胞占有,利用均摊法计算晶胞化学式;
解答:解:根据晶胞的结构可知,晶胞中位于顶点的X离子有4个,位于立方体顶点的X离子被8个晶胞共有,所以一个晶胞中含有X离子
×4=
;
位于体心的离子Y有1个,位于立方体中心的Y离子被一个晶胞占有,所以X和Y离子的个数比为
:1=1:2,
所以化学式为XY2或Y2X.
故答案为:XY2或Y2X.
| 1 |
| 8 |
| 1 |
| 2 |
位于体心的离子Y有1个,位于立方体中心的Y离子被一个晶胞占有,所以X和Y离子的个数比为
| 1 |
| 2 |
所以化学式为XY2或Y2X.
故答案为:XY2或Y2X.
点评:本题考查了根据晶胞结构确定化学式,难度不大,利用均摊法即可分析解答本题.

练习册系列答案
相关题目
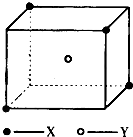 某离子晶体晶胞结构如图所示,X位于立方体的顶点,Y位于立方体中心.试分析:
某离子晶体晶胞结构如图所示,X位于立方体的顶点,Y位于立方体中心.试分析: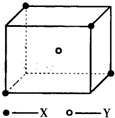 某离子晶体晶胞结构如图所示,x位于立方体的顶点,Y位于立方体中心.试分析:每个x同时吸引着
某离子晶体晶胞结构如图所示,x位于立方体的顶点,Y位于立方体中心.试分析:每个x同时吸引着