题目内容
下列对于合金性质的叙述不正确的是( )
| A.合金的熔点低于它的任何一种成分金属的熔点 |
| B.合金的硬度一般比各成分金属的硬度都大 |
| C.合金的密度小于各成分金属的密度 |
| D.合金的导电性、导热性比各成分金属低 |
C
合金有如下三个特征:熔沸点一般比任一组分低,硬度比任一组分大,密度介于两者之间。故不正确的叙述为C选项。

练习册系列答案
 金版课堂课时训练系列答案
金版课堂课时训练系列答案 单元全能练考卷系列答案
单元全能练考卷系列答案 新黄冈兵法密卷系列答案
新黄冈兵法密卷系列答案
相关题目
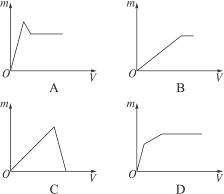
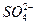 ,向含a mol KAl(SO4)2的溶液中,逐滴加入Ba(OH)2溶液,过程中可能存在以下多个离子方程式
,向含a mol KAl(SO4)2的溶液中,逐滴加入Ba(OH)2溶液,过程中可能存在以下多个离子方程式
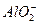 +2H2O
+2H2O