题目内容
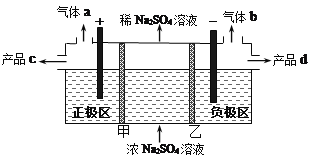
【题目】三室式电渗析法处理含Na2SO4废水的原理如图所示,采用惰性电极,甲、乙均为离子交换膜,在直流电场的作用下,两膜中间的Na+和SO42-可通过离子交换膜,而两端隔室中离子被阻挡不能进入中间隔室。下列叙述正确的是
A. 甲为阳离子交换膜,通电后中间隔室的Na+离子向正极迁移
B. 通电后,同温同压下得到的气体a与气体b的体积比约为2:1
C. 通电后,得到的产品c是NaOH,产品d是H2SO4
D. 负极区发生的电极反应为2H2O +2e-=2OH-+H2↑,负极区溶液pH增大
【答案】D
【解析】在负极区发生的电极反应为2H2O +2e-=2OH-+H2↑,负极区氢氧根离子浓度增大,钠离子向负极区移动,达到溶液电荷守恒;在正极区发生的电极反应为2H2O -4e-=4H++O2↑,硫酸根离子向正极区移动。A. 甲为阴离子交换膜,通电后中间隔室的硫酸根离子向正极迁移,A错误;B. 通电后,同温同压下得到的气体O2与气体H2的体积比约为1:2,B错误;C. 通电后,得到的产品d是NaOH,产品c是H2SO4,C错误;D. 负极区发生的电极反应为2H2O +2e-=2OH-+H2↑,负极区氢氧根离子浓度增大,溶液pH增大,D正确;故答案选D。

练习册系列答案
 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案
相关题目